Wykres Rozpuszczalności Soli
Czy kiedykolwiek zastanawiałeś się, dlaczego cukier łatwiej rozpuszcza się w ciepłej herbacie niż w zimnej? A może próbowałeś nasypać zbyt dużo soli do roztworu i zauważyłeś, że dalsze dodawanie już nic nie daje? Odpowiedź na te pytania kryje się w wykresach rozpuszczalności soli – narzędziach, które pozwalają nam zrozumieć, jak temperatura wpływa na to, ile danej substancji możemy rozpuścić w wodzie.
W życiu codziennym, od gotowania po czyszczenie, proces rozpuszczania substancji odgrywa kluczową rolę. Zrozumienie, co wpływa na rozpuszczalność, pozwala nam efektywniej korzystać z roztworów i unikać niepotrzebnych problemów. Wyobraź sobie, że przygotowujesz roztwór do podlewania roślin. Użycie zbyt mocnego stężenia nawozu (rozpuszczonego w wodzie) może im zaszkodzić. Wiedza o rozpuszczalności pozwoli Ci uniknąć tej pomyłki.
Czym jest Wykres Rozpuszczalności Soli?
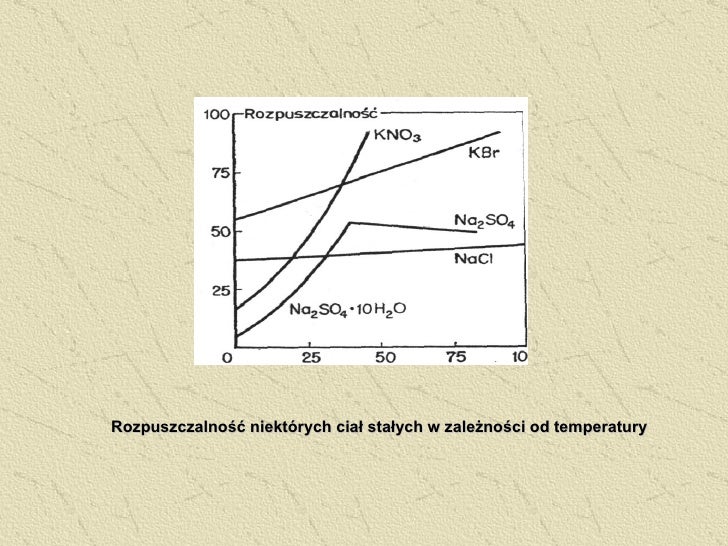
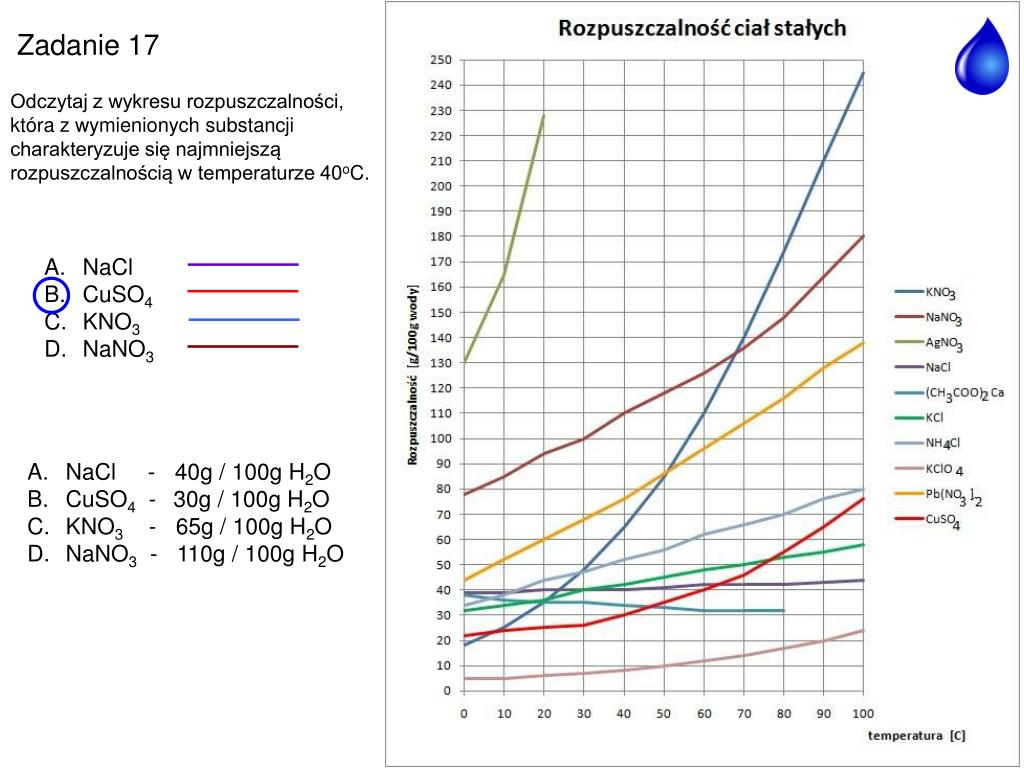
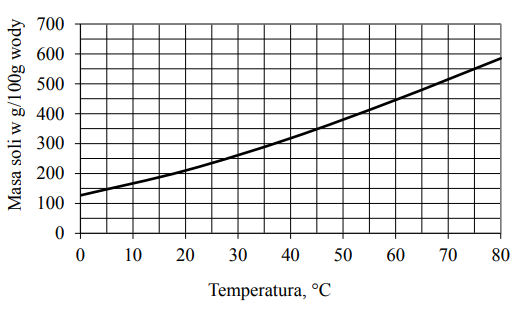
Wykres rozpuszczalności soli to graficzne przedstawienie zależności między rozpuszczalnością danej soli w wodzie a temperaturą. Mówiąc prościej, pokazuje nam, ile gramów danej soli można maksymalnie rozpuścić w 100 gramach wody w określonej temperaturze. Wykresem jest zwykle linia (krzywa), gdzie oś X przedstawia temperaturę (zwykle w stopniach Celsjusza), a oś Y rozpuszczalność (zwykle w gramach soli na 100g wody).
Każda sól ma swój unikalny wykres rozpuszczalności. Niektóre sole, jak na przykład azotan potasu (KNO3), wykazują znaczący wzrost rozpuszczalności wraz ze wzrostem temperatury. Inne, jak chlorek sodu (NaCl, czyli zwykła sól kuchenna), mają rozpuszczalność, która zmienia się w niewielkim stopniu w zależności od temperatury.
Jak czytać Wykres Rozpuszczalności?
Czytanie wykresu rozpuszczalności jest proste, ale wymaga pewnej uwagi. Oto kilka kroków:
- Znajdź interesującą Cię temperaturę na osi X.
- Poprowadź linię pionową od tej temperatury aż do punktu przecięcia z krzywą rozpuszczalności danej soli.
- Poprowadź linię poziomą od punktu przecięcia do osi Y.
- Odczytaj wartość na osi Y – to jest rozpuszczalność danej soli w gramach na 100g wody w wybranej temperaturze.
Przykład: Załóżmy, że chcesz sprawdzić, jaka jest rozpuszczalność azotanu potasu w 50°C. Znajdujesz na wykresie punkt odpowiadający 50°C, wędrujesz pionowo do góry aż do krzywej KNO3, a następnie poziomo w lewo. Odczytana wartość na osi Y (przyjmijmy, że to 85g/100g wody) oznacza, że w 50°C w 100 gramach wody można rozpuścić maksymalnie 85 gramów azotanu potasu.
Co oznaczają punkty na wykresie?
- Punkty leżące na krzywej: Oznaczają roztwór nasycony. Oznacza to, że roztwór zawiera maksymalną ilość soli, jaką można rozpuścić w danej temperaturze. Dodanie kolejnej porcji soli spowoduje, że nie rozpuści się ona, tylko osadzi na dnie naczynia.
- Punkty leżące poniżej krzywej: Oznaczają roztwór nienasycony. Oznacza to, że roztwór zawiera mniej soli, niż jest to możliwe do rozpuszczenia w danej temperaturze. Można dodać więcej soli, a ona się rozpuści.
- Punkty leżące powyżej krzywej: Teoretycznie oznaczają roztwór przesycony. Takie roztwory są niestabilne i powstają w specyficznych warunkach (np. powolne ochładzanie nasyconego roztworu bez obecności kryształków soli). Dodanie nawet małego kryształku soli do takiego roztworu spowoduje krystalizację nadmiaru soli i powrót do stanu nasycenia.
Dlaczego Rozpuszczalność zależy od Temperatury?
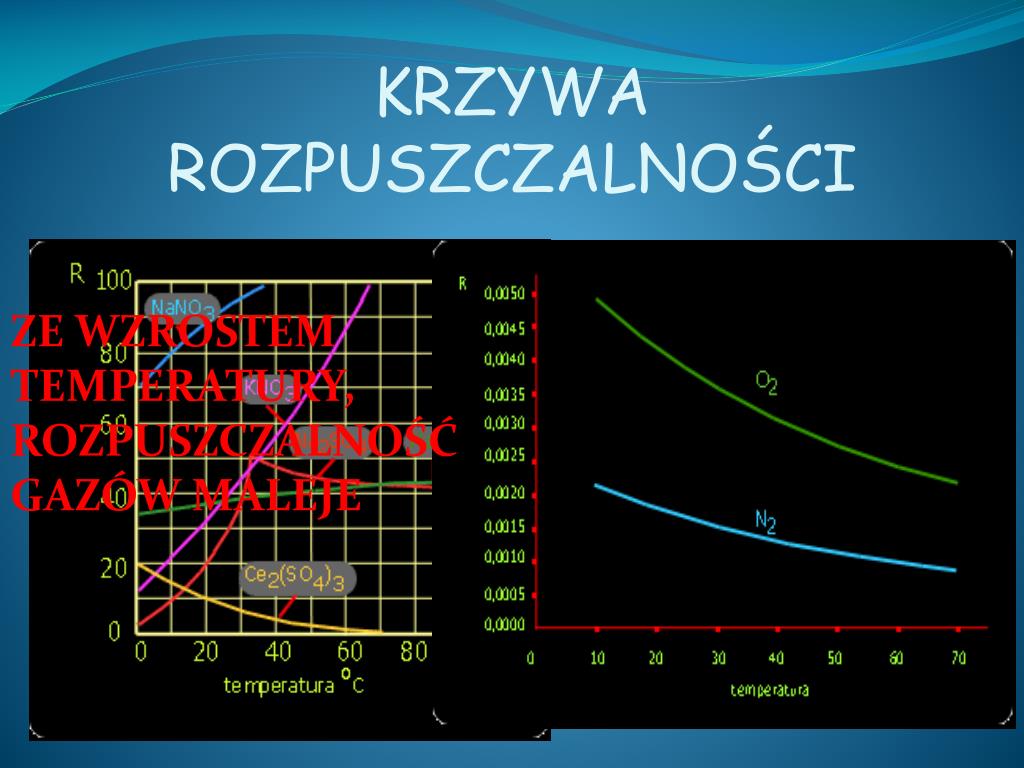
Zazwyczaj, choć nie zawsze, rozpuszczalność ciał stałych, takich jak sole, wzrasta wraz ze wzrostem temperatury. Dlaczego tak się dzieje? Proces rozpuszczania jest związany z pokonywaniem sił przyciągania między cząsteczkami soli oraz sił między cząsteczkami wody. Podwyższenie temperatury dostarcza energii kinetycznej cząsteczkom wody i soli, co ułatwia im pokonywanie tych sił i mieszanie się ze sobą. Wyjątkiem od tej reguły są niektóre sole, których rozpuszczalność maleje wraz ze wzrostem temperatury.
Przykładowo, roztwór nasycony azotanu potasu (KNO3) w temperaturze pokojowej zawiera znacznie mniej soli niż roztwór nasycony w temperaturze 80°C. Można to wykorzystać do krystalizacji azotanu potasu: przygotowujemy nasycony roztwór w wysokiej temperaturze, a następnie powoli ochładzamy go. Wraz ze spadkiem temperatury, rozpuszczalność azotanu potasu maleje, co powoduje, że sól krystalizuje się z roztworu.
Praktyczne Zastosowania Wykresów Rozpuszczalności
Wykresy rozpuszczalności mają szerokie zastosowanie w różnych dziedzinach:
- Chemia laboratoryjna: Pomagają w przygotowywaniu roztworów o określonym stężeniu, niezbędnych do przeprowadzania eksperymentów i analiz.
- Przemysł farmaceutyczny: Pozwalają na optymalizację procesu wytwarzania leków, gdzie rozpuszczalność substancji czynnych ma kluczowe znaczenie dla ich skuteczności.
- Przemysł spożywczy: Wykorzystywane są w procesach krystalizacji cukru, produkcji soli kuchennej i innych produktów.
- Rolnictwo: Pomagają w doborze odpowiednich nawozów i ich stężeń, aby zapewnić roślinom optymalne warunki wzrostu.
- Edukacja: Są doskonałym narzędziem do nauki o roztworach, rozpuszczalności i czynnikach, które na nią wpływają.
Przykład z życia wzięty: Przygotowując dżem, dodajemy cukier do owoców i podgrzewamy mieszaninę. Podgrzewanie zwiększa rozpuszczalność cukru, co pozwala na uzyskanie bardziej skoncentrowanego roztworu cukru, a tym samym na lepszą konserwację owoców. Kucharze i cukiernicy instynktownie wykorzystują zasady rozpuszczalności, choć często nie zdają sobie sprawy z teorii, która za tym stoi.
Źródła Danych o Rozpuszczalności
Skąd brać dane do tworzenia lub odczytywania wykresów rozpuszczalności? Istnieje wiele wiarygodnych źródeł:
- Tablice chemiczne: Znajdziesz w nich dane o rozpuszczalności wielu substancji w różnych temperaturach. Podręczniki chemii analitycznej i fizycznej często zawierają obszerne tablice rozpuszczalności.
- Bazy danych online: Istnieją specjalistyczne bazy danych, takie jak ChemSpider czy PubChem, które zawierają informacje o właściwościach fizykochemicznych, w tym o rozpuszczalności.
- Artykuły naukowe: Wyniki badań dotyczących rozpuszczalności są często publikowane w czasopismach naukowych.
Podsumowanie
Wykresy rozpuszczalności soli są potężnym narzędziem, które pomaga nam zrozumieć, jak temperatura wpływa na rozpuszczalność substancji. Pozwalają nam przewidywać, ile soli można rozpuścić w danej ilości wody w określonej temperaturze, co jest kluczowe w wielu dziedzinach, od chemii laboratoryjnej po przemysł spożywczy. Zrozumienie wykresów rozpuszczalności pozwala na bardziej efektywne i świadome wykorzystywanie roztworów w życiu codziennym i w pracy zawodowej.
Mamy nadzieję, że ten artykuł pomógł Ci lepiej zrozumieć, czym są wykresy rozpuszczalności soli i jak je wykorzystywać. Pamiętaj, że zdobyta wiedza otwiera drzwi do lepszego zrozumienia świata chemii i procesów, które zachodzą wokół nas każdego dnia.