Wskaż Wzory Sumaryczne Kwasów Beztlenowych

Hej! Gotowi na małą chemiczną przygodę? Dzisiaj pod lupę bierzemy kwasy beztlenowe! Bez obaw, nie będziemy grzebać w skomplikowanych tablicach Mendelejewa (no, może tylko zerknąć!). Spróbujemy zrozumieć, jak zapisać te kwasy tak, żeby wyglądało to… no, jak przepis na ciasto! Tylko zamiast mąki i cukru, będziemy mieli atomy!
Co to właściwie są te kwasy beztlenowe?
Wyobraź sobie, że kwasy to takie złośliwe chochliki, które uwielbiają reagować z innymi substancjami. Kwasy beztlenowe to te chochliki, które do swojej złośliwej pracy nie potrzebują tlenu! To jak kucharz, który potrafi upiec pyszne ciasto bez jajek – imponujące, prawda? Najważniejsze to zapamiętać, że te kwasy składają się z wodoru (H) i jakiegoś niemetalu.
No dobra, ale jak to zapisać?
Wzór sumaryczny kwasu beztlenowego jest prosty jak budowa cepa (przepraszam, cepy!). Zawsze zaczynamy od wodoru (H). Następnie dodajemy symbol niemetalu, który tworzy z nim kwas. I już! Prawie…
Kluczem jest odpowiednie dobranie ilości atomów wodoru, tak żeby wszystko się "zgadzało". Bo, jak wiemy, chemia lubi porządek! Każdy niemetal ma swoją "wartościowość" – to takie jego supermoce łączenia się z innymi atomami. Wodór jest zazwyczaj jednowartościowy.
Przykłady, przykłady, chcemy przykłady!
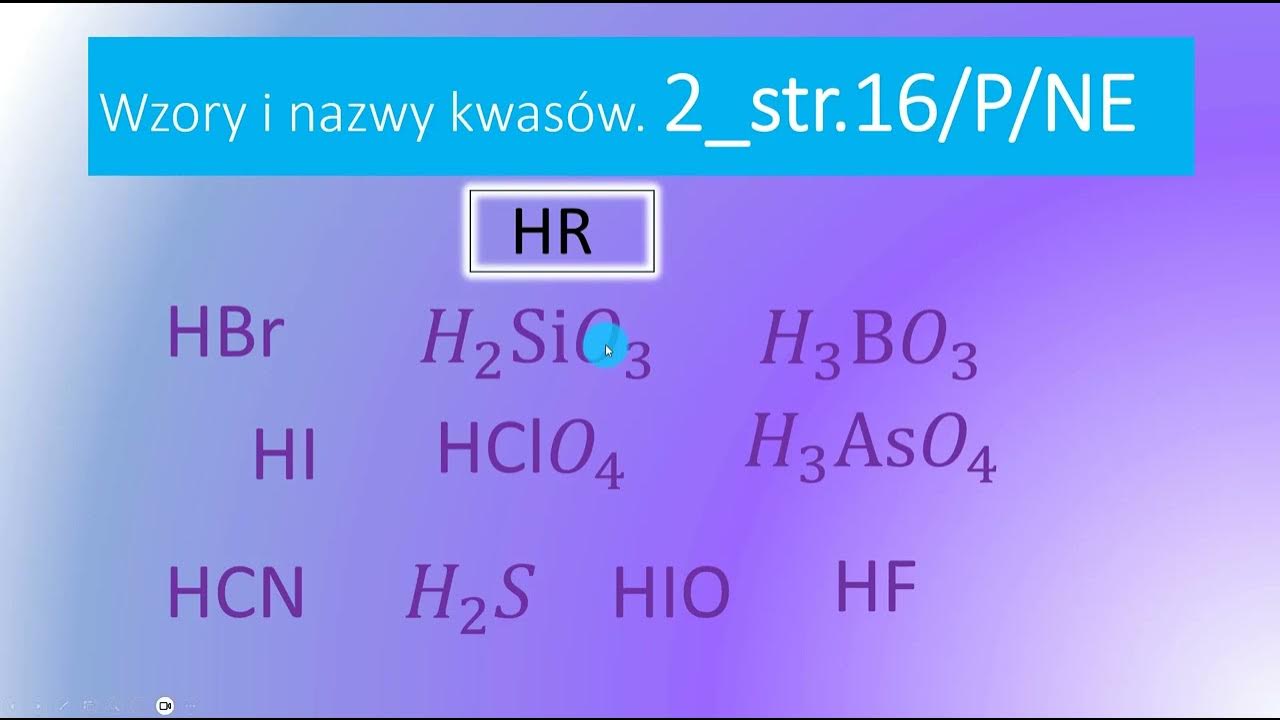
Okej, oto kilka przepisów na kwasy beztlenowe, podanych w formie wzorów sumarycznych:
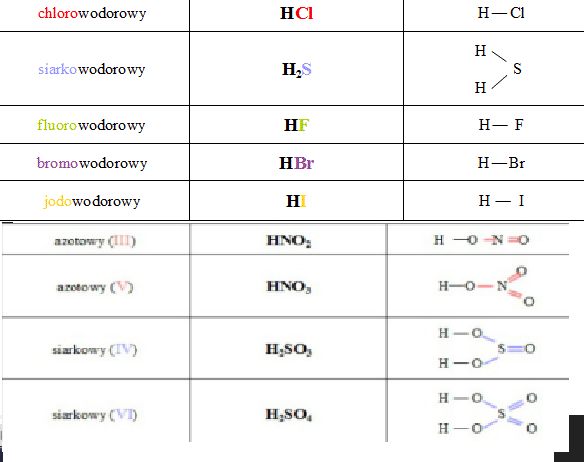
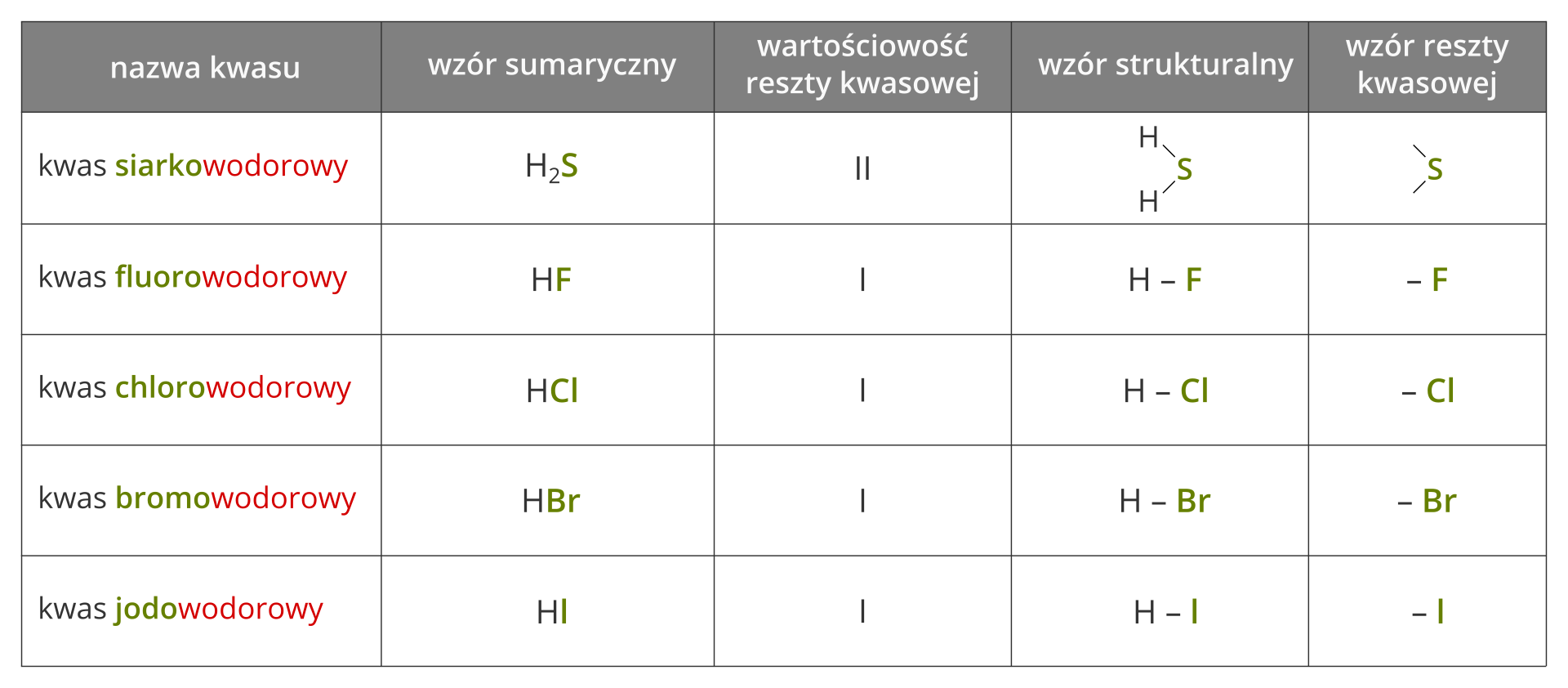
- Kwas chlorowodorowy (HCl): To chyba najpopularniejszy kwas beztlenowy! Wodór (H) łączy się z chlorem (Cl). Chlorek jest jednowartościowy, więc potrzebujemy jednego wodoru. Proste, prawda? To tak, jakby jeden kot łapał jedną mysz!
- Kwas bromowodorowy (HBr): Podobnie jak wyżej, wodór (H) łączy się z bromem (Br). Brom również jest jednowartościowy, więc znowu jeden wodór wystarczy. To jak jedno dziecko dostaje jednego cukierka – sprawiedliwość musi być!
- Kwas jodowodorowy (HI): Widzicie schemat? Wodór (H) plus jod (I). Jod też jednowartościowy. Czyli… H + I = HI! Brawo Wy! Już jesteście mistrzami w pisaniu wzorów!
- Kwas siarkowodorowy (H2S): A tutaj mała niespodzianka! Siarka (S) jest dwuwartościowa, co oznacza, że potrzebuje dwóch atomów wodoru, żeby stworzyć stabilny związek. Dlatego wzór to H2S. To jakby jeden wielki pies potrzebował dwóch smyczy, żeby nikt nie uciekł!
Zauważyliście, że we wzorach najważniejsze jest, żeby suma "wartościowości" atomów wodoru zgadzała się z "wartościowością" niemetalu. To jak układanka – wszystkie elementy muszą pasować do siebie!
Kilka słów na koniec
Pamiętajcie, wzory sumaryczne kwasów beztlenowych to nie czarna magia! To po prostu zapis, który pokazuje, z jakich atomów i w jakich proporcjach składa się dany kwas. A teraz idźcie i zadziwiajcie świat swoją wiedzą chemiczną! I pamiętajcie, chemia może być naprawdę fajna, tylko trzeba do niej podejść z uśmiechem!
Aha, i nie próbujcie robić tych kwasów w domu, chyba że macie supernowoczesne laboratorium i doktorat z chemii. Bezpieczeństwo przede wszystkim!