Woda I Roztwory Wodne Sprawdzian Klasa 7

Hej siódmoklasisto! Przed Tobą sprawdzian z wody i roztworów wodnych? Bez obaw! Jestem tutaj, żeby Ci pomóc. Przygotowałem dla Ciebie ten przewodnik, który krok po kroku przypomni najważniejsze informacje i zagadnienia. Pamiętaj, nauka nie musi być straszna, a dobrze opanowany materiał to klucz do sukcesu. Zacznijmy!
Woda – Niezwykła Substancja
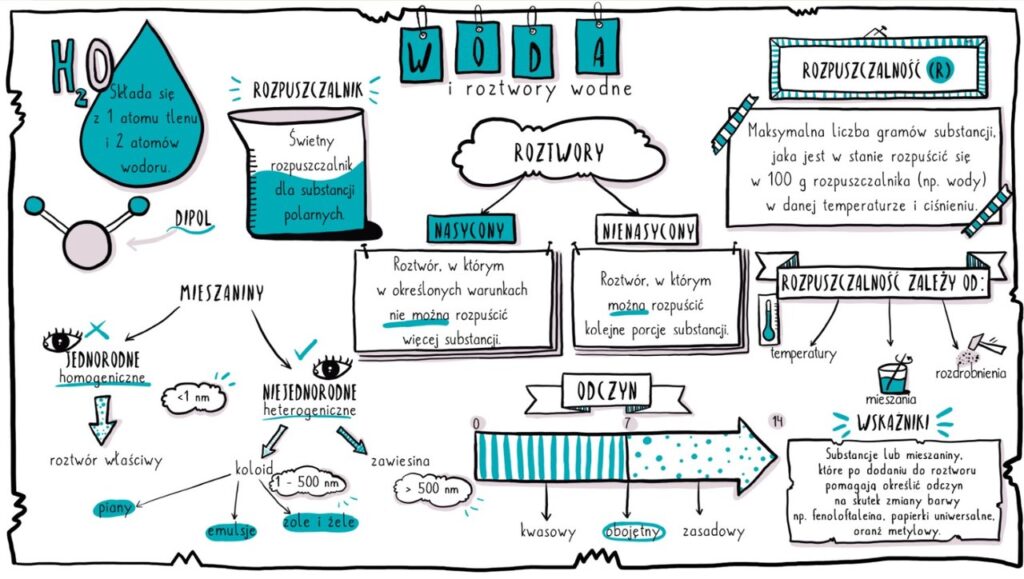
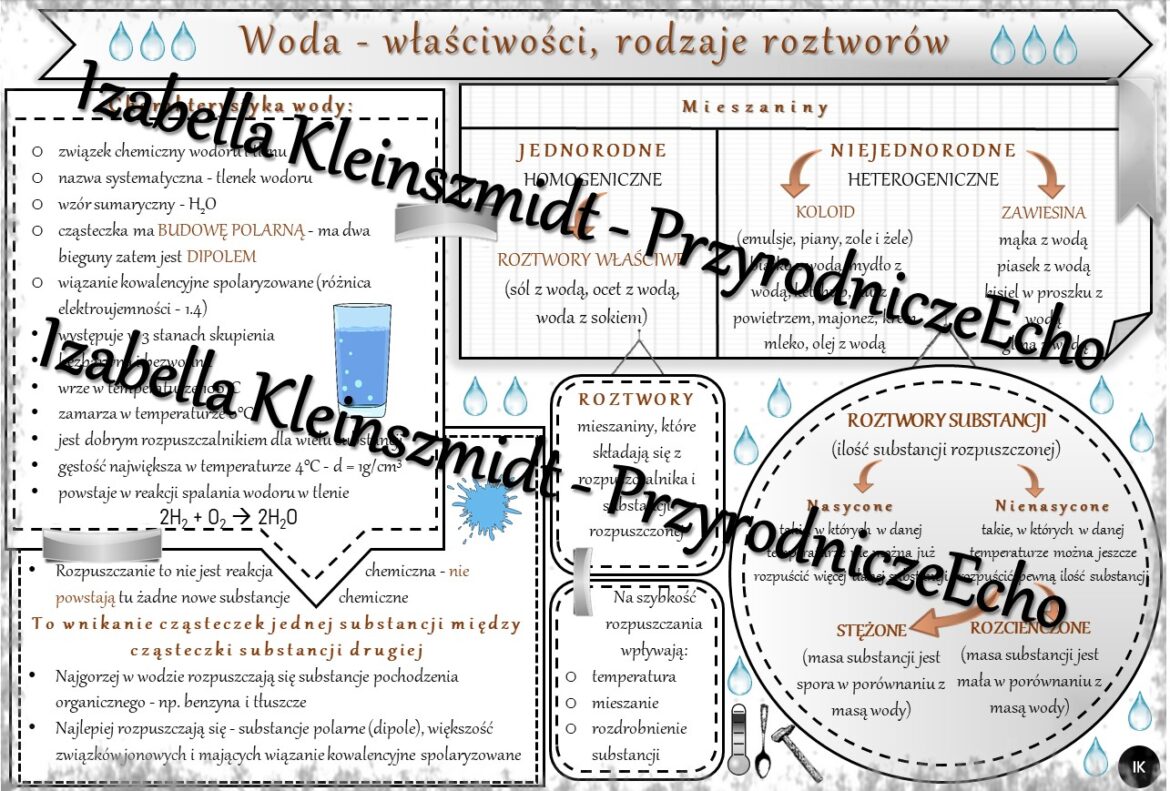
Woda to podstawa życia na Ziemi. To rozpuszczalnik, który odgrywa kluczową rolę w wielu procesach biologicznych i chemicznych. Zanim przejdziemy do roztworów, przypomnijmy sobie kilka podstawowych faktów o wodzie:
- Wzór chemiczny: H2O (dwa atomy wodoru i jeden atom tlenu)
- Stan skupienia: Występuje w trzech stanach skupienia: stałym (lód), ciekłym (woda) i gazowym (para wodna).
- Właściwości fizyczne: Bezbarwna, bezwonna i bez smaku (w czystej postaci). Ma wysokie ciepło właściwe, co oznacza, że potrzebuje dużo energii, żeby się ogrzać lub ochłodzić.
- Rola w przyrodzie: Niezbędna do życia roślin i zwierząt, reguluje klimat, transportuje składniki odżywcze.
Zwróć uwagę na polarność cząsteczki wody. Atom tlenu jest bardziej elektroujemny niż atomy wodoru, co powoduje, że cząsteczka wody ma częściowy ładunek ujemny przy tlenie i częściowe ładunki dodatnie przy wodorach. To właśnie polarność sprawia, że woda jest tak dobrym rozpuszczalnikiem dla wielu substancji.
Pytania kontrolne:
1. Jakie są trzy stany skupienia wody?
2. Co to znaczy, że woda jest polarna?
3. Dlaczego woda jest tak ważna dla życia?
Roztwory Wodne – Mieszaniny Jednorodne
Teraz przejdźmy do roztworów wodnych. Roztwór to mieszanina jednorodna dwóch lub więcej substancji. Oznacza to, że na pierwszy rzut oka nie widać, z czego się składa. W roztworze wodnym rozpuszczalnikiem jest woda, a substancją rozpuszczaną – substancja, która się w niej rozpuszcza (np. sól, cukier).
Rodzaje roztworów:
- Roztwór nienasycony: Można jeszcze rozpuścić w nim więcej substancji.
- Roztwór nasycony: Nie można już rozpuścić więcej substancji w danej temperaturze.
- Roztwór przesycony: Zawiera więcej substancji rozpuszczonej niż roztwór nasycony w danej temperaturze. Roztwory przesycone są nietrwałe i łatwo wytrącają się z nich kryształy.
Rozpuszczalność
Rozpuszczalność to zdolność danej substancji do rozpuszczania się w rozpuszczalniku. Zależy od rodzaju substancji, rozpuszczalnika oraz temperatury. Zazwyczaj, im wyższa temperatura, tym więcej substancji można rozpuścić w wodzie (szczególnie dotyczy to substancji stałych).
Ważne! Niektóre substancje rozpuszczają się w wodzie bardzo dobrze (np. sól kuchenna), inne słabo (np. piasek), a jeszcze inne wcale (np. olej).
Pytania kontrolne:
1. Co to jest roztwór?
2. Jakie są rodzaje roztworów?
3. Od czego zależy rozpuszczalność substancji?
Stężenie Procentowe Roztworu (Cp)
Stężenie procentowe roztworu (Cp) to wyrażony w procentach stosunek masy substancji rozpuszczonej do masy całego roztworu. Innymi słowy, mówi nam, ile gramów substancji znajduje się w 100 gramach roztworu. Wzór na stężenie procentowe:
Cp = (ms / mr) * 100%
Gdzie:
- Cp - stężenie procentowe
- ms - masa substancji rozpuszczonej (w gramach)
- mr - masa roztworu (w gramach)
Masa roztworu (mr) to suma masy substancji rozpuszczonej (ms) i masy rozpuszczalnika (mw) (w tym przypadku wody):
mr = ms + mw
Przykład:
Rozpuszczono 20g cukru w 80g wody. Oblicz stężenie procentowe roztworu.
- ms = 20g (masa cukru)
- mw = 80g (masa wody)
- mr = ms + mw = 20g + 80g = 100g (masa roztworu)
- Cp = (ms / mr) * 100% = (20g / 100g) * 100% = 20%
Odpowiedź: Stężenie procentowe roztworu wynosi 20%.
Jak przygotować roztwór o danym stężeniu?
Żeby przygotować roztwór o danym stężeniu, musisz obliczyć odpowiednią ilość substancji rozpuszczonej i rozpuszczalnika. Możesz to zrobić, przekształcając wzór na stężenie procentowe.
Pytania kontrolne:
1. Co to jest stężenie procentowe roztworu?
2. Jaki jest wzór na stężenie procentowe?
3. Jak obliczyć masę roztworu?
Podsumowanie
Gratulacje! Przeszliśmy przez najważniejsze zagadnienia dotyczące wody i roztworów wodnych. Przypomnijmy sobie najważniejsze punkty:
- Woda to niezwykły rozpuszczalnik, niezbędny do życia.
- Roztwór to mieszanina jednorodna.
- Rozróżniamy roztwory nienasycone, nasycone i przesycone.
- Rozpuszczalność zależy od rodzaju substancji, rozpuszczalnika i temperatury.
- Stężenie procentowe (Cp) określa, ile gramów substancji znajduje się w 100 gramach roztworu.
Pamiętaj, żeby poćwiczyć rozwiązywanie zadań ze stężeniem procentowym! Im więcej przykładów przeanalizujesz, tym lepiej zrozumiesz ten temat.
Powodzenia na sprawdzianie! Wierzę w Ciebie!