Substancja Chemiczna łącząca Się Z Inną W Reakcji Syntezy

Witajcie! Dzisiaj porozmawiamy o tych substancjach chemicznych, które łączą się ze sobą w reakcjach syntezy. To tak jak budowanie czegoś z klocków – mamy różne klocki (substancje) i łączymy je, aby stworzyć coś nowego i większego.
Wyobraźcie sobie, że macie dwa rodzaje klocków LEGO: czerwone i niebieskie. Reakcja syntezy to jak połączenie jednego czerwonego klocka z jednym niebieskim, żeby powstał klocek fioletowy (trochę upraszczając, ale to dobry obraz!). W chemii te "klocki" to atomy lub cząsteczki, a "fioletowy klocek" to nowy związek chemiczny, który powstał w wyniku reakcji.
Zatem, co to za substancje? To po prostu reagenty. Reagenty to te substancje, które wchodzą w reakcję chemiczną. Są to składniki, które "startują" reakcję syntezy i przekształcają się w produkt lub produkty. Myślcie o nich jak o składnikach przepisu kulinarnego. Bez nich nie przygotujecie dania.
Przykłady Reakcji Syntezy
Żeby lepiej to zrozumieć, przyjrzyjmy się kilku przykładom.
-
Tworzenie wody (H₂O): Najprostszy przykład to połączenie wodoru (H₂) z tlenem (O₂). Dwa atomy wodoru łączą się z jednym atomem tlenu, tworząc cząsteczkę wody. Równanie reakcji wygląda tak: 2H₂ + O₂ → 2H₂O. Wodór i tlen to nasze reagenty, a woda to produkt.
-
Powstawanie chlorku sodu (NaCl) – soli kuchennej: Sód (Na) reaguje z chlorem (Cl₂), tworząc chlorek sodu. Równanie reakcji: 2Na + Cl₂ → 2NaCl. Sód i chlor to reagenty, a chlorek sodu to produkt.
-
Synteza amoniaku (NH₃) – proces Habera-Boscha: To bardzo ważny proces w przemyśle, ponieważ amoniak jest używany do produkcji nawozów. Wodór (H₂) reaguje z azotem (N₂), tworząc amoniak. Równanie reakcji: N₂ + 3H₂ → 2NH₃. Azot i wodór to reagenty, a amoniak to produkt.
-
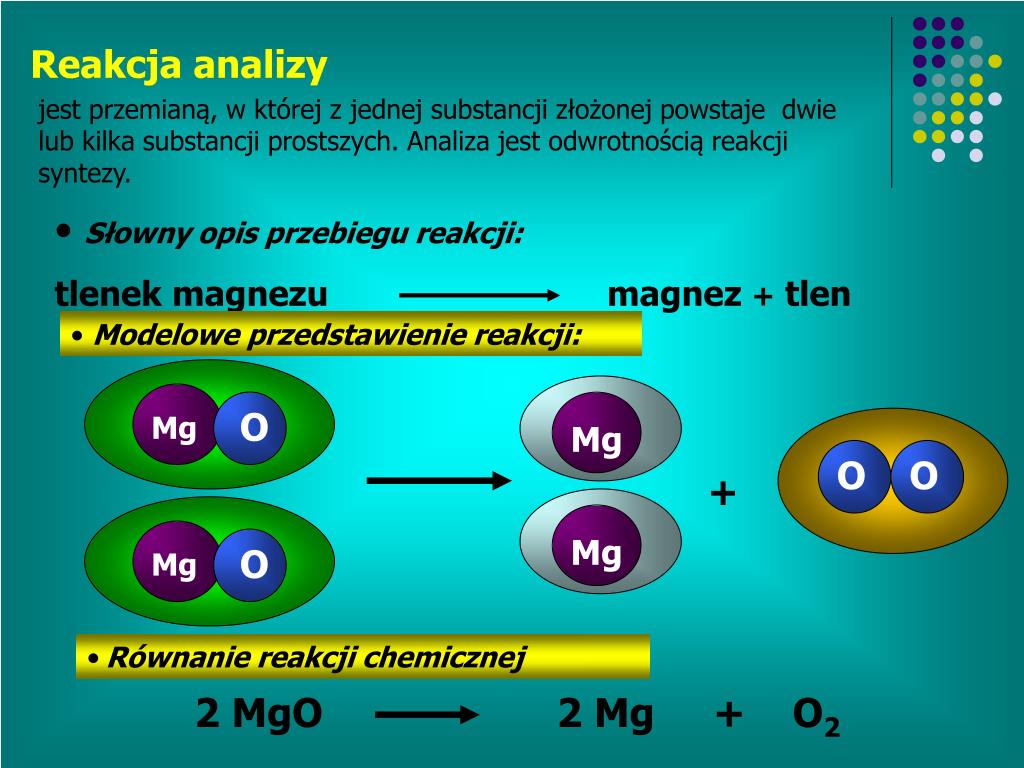
Tworzenie tlenku magnezu (MgO): Magnez (Mg) reaguje z tlenem (O₂), tworząc tlenek magnezu. Równanie reakcji: 2Mg + O₂ → 2MgO. Magnez i tlen to reagenty, a tlenek magnezu to produkt. Tlenek magnezu powstaje np. podczas spalania magnezu – widzimy wtedy jasny, oślepiający płomień.
Jak widzicie, w każdej z tych reakcji mamy dwie (lub więcej) substancje, które ze sobą reagują – to właśnie reagenty. One "znikają" (przekształcają się), a w ich miejsce pojawia się nowa substancja – produkt.
Jak Rozpoznać Reakcję Syntezy?
Najprościej po tym, że kilka substancji łączy się w jedną. Spójrzcie na równanie reakcji. Jeśli po lewej stronie (przed strzałką) macie kilka składników, a po prawej stronie (po strzałce) tylko jeden, to najprawdopodobniej macie do czynienia z reakcją syntezy. Oczywiście, czasami reakcje mogą być bardziej skomplikowane i zachodzić w kilku etapach, ale ogólna zasada jest taka sama: proste elementy łączą się w coś bardziej złożonego.
Rodzaje Reakcji Syntezy
Reakcje syntezy można podzielić na kilka rodzajów, w zależności od tego, jakie substancje ze sobą reagują.
-
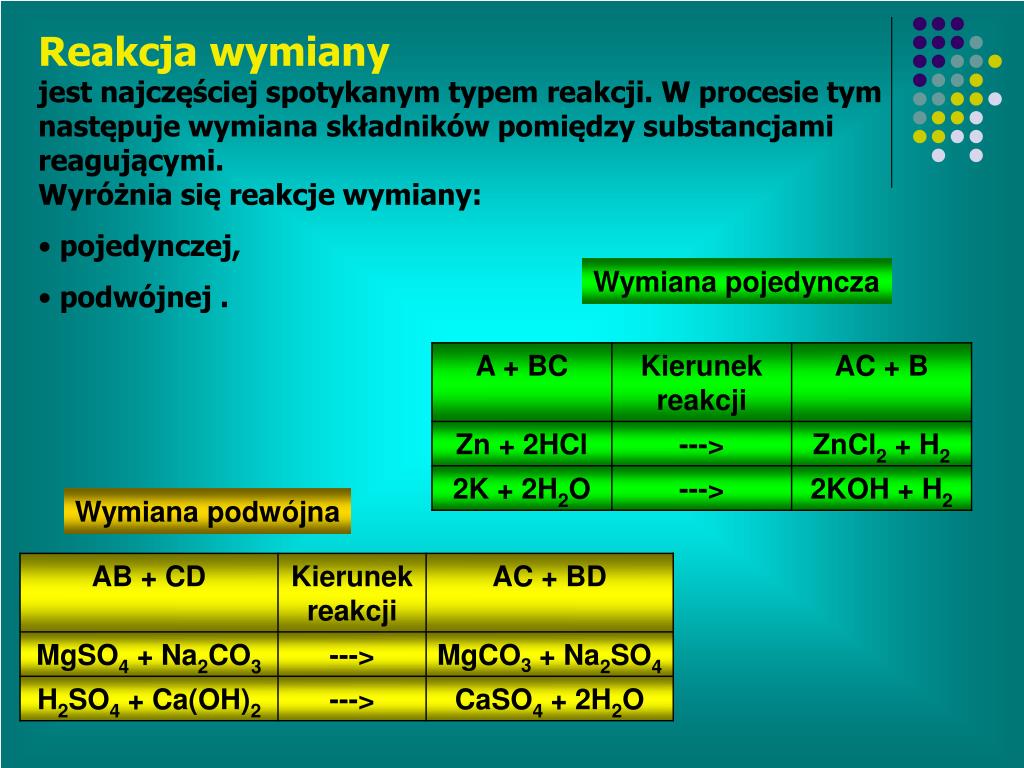
Reakcja bezpośrednia: To najprostszy typ syntezy, gdzie dwa pierwiastki lub związki łączą się bezpośrednio, tworząc jeden nowy związek. Przykładem jest reakcja sodu z chlorem, tworząca chlorek sodu.
-
Reakcja addycji: W tym przypadku, jeden związek przyłącza się do drugiego, bez odłączania żadnych atomów. Często zachodzi w związkach organicznych, np. przyłączenie wodoru do alkenu (związku z wiązaniem podwójnym).
-
Reakcja polimeryzacji: W tej reakcji wiele małych cząsteczek (monomerów) łączy się ze sobą, tworząc dużą cząsteczkę (polimer). Przykładem jest tworzenie polietylenu z etylenu.
Znaczenie Reakcji Syntezy
Reakcje syntezy są niezwykle ważne w chemii i przemyśle. Dzięki nim możemy tworzyć nowe materiały, leki, nawozy, tworzywa sztuczne i wiele innych produktów, które są niezbędne w naszym codziennym życiu. Bez reakcji syntezy nie byłoby możliwe wytwarzanie wielu substancji, które są dla nas oczywiste. Na przykład, synteza amoniaku (proces Habera-Boscha) umożliwiła produkcję nawozów na skalę przemysłową, co zrewolucjonizowało rolnictwo i pozwoliło na wyżywienie większej liczby ludzi.
Dlaczego Reakcje Syntezy Zachodzą?
Reakcje syntezy, jak każda reakcja chemiczna, zachodzą dlatego, że produkty reakcji są bardziej stabilne (mają niższą energię) niż reagenty. Dążenie do obniżenia energii jest podstawową zasadą w chemii. Żeby reakcja zaszła, czasami potrzebna jest energia aktywacji – taka "iskra", która zapoczątkuje reakcję. Może to być ciepło, światło lub katalizator. Katalizator to substancja, która przyspiesza reakcję, ale sama nie ulega zużyciu. Myślcie o katalizatorze jak o pomocniku, który ułatwia reagującym substancjom połączenie się.
Podsumowanie
Reagenty to substancje chemiczne, które łączą się ze sobą w reakcjach syntezy, tworząc nowe związki chemiczne – produkty. Reakcje syntezy są podstawą chemii i przemysłu, umożliwiając tworzenie wielu niezbędnych substancji. Rozpoznajemy je po tym, że kilka substancji łączy się w jedną. Pamiętajcie o przykładach, które omówiliśmy: tworzenie wody, soli kuchennej, amoniaku i tlenku magnezu. Dzięki temu łatwiej zapamiętacie, czym są reagenty i jak zachodzą reakcje syntezy.
Mam nadzieję, że teraz lepiej rozumiecie, co to są reagenty w reakcjach syntezy! Powodzenia w dalszej nauce chemii!