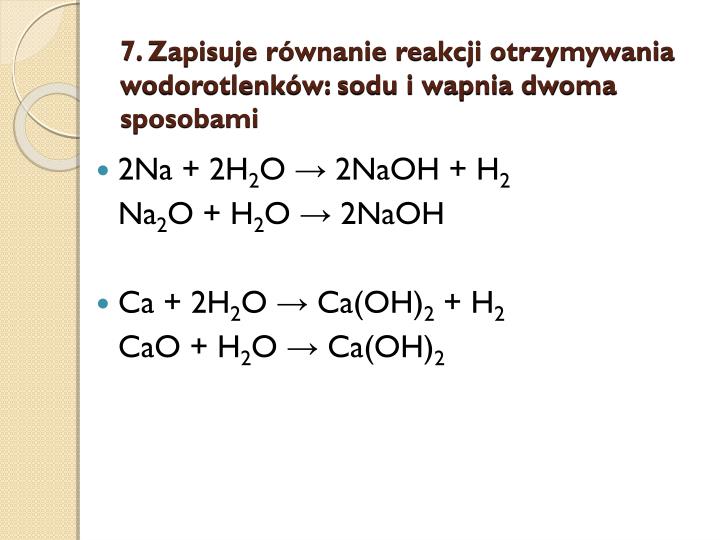
Otrzymywanie Wodorotlenku Sodu

Czy kiedykolwiek zastanawiałeś się, jak powstaje wodorotlenek sodu (NaOH), substancja obecna w tak wielu produktach, od środków czyszczących po papier? Być może myślisz, że to skomplikowany proces dostępny tylko dla profesjonalnych chemików. Choć produkcja na skalę przemysłową wymaga zaawansowanej technologii, zrozumienie podstawowych metod otrzymywania NaOH jest dostępne dla każdego. Spróbujemy to wyjaśnić w prosty i przystępny sposób.
Co to jest Wodorotlenek Sodu i Dlaczego Jest Ważny?
Wodorotlenek sodu, znany również jako soda kaustyczna lub ług sodowy, to silna zasada nieorganiczna. Jego wzór chemiczny to NaOH. Jest to biała, higroskopijna substancja stała, która rozpuszcza się w wodzie z wydzieleniem dużej ilości ciepła. Jest niezwykle reaktywny i znajduje zastosowanie w wielu gałęziach przemysłu. Od produkcji mydła po oczyszczanie ścieków – NaOH odgrywa kluczową rolę.
Według raportu "Global Sodium Hydroxide (Caustic Soda) Market Analysis 2024" globalny rynek wodorotlenku sodu stale rośnie, co świadczy o jego niezbędności w wielu procesach produkcyjnych. Bez niego wiele aspektów naszego życia, od czystości w domu po produkcję leków, byłoby znacznie utrudnionych.
Metody Otrzymywania Wodorotlenku Sodu
Istnieją głównie trzy przemysłowe metody otrzymywania wodorotlenku sodu. Każda z nich bazuje na elektrolizie roztworu chlorku sodu (soli kuchennej) i różni się zastosowanymi technologiami:
1. Metoda rtęciowa
Metoda rtęciowa, historycznie najstarsza, polega na elektrolizie roztworu NaCl z użyciem katody rtęciowej. W wyniku elektrolizy na katodzie powstaje amalgamat sodu (stop sodu z rtęcią), który następnie reaguje z wodą, tworząc wodorotlenek sodu i odzyskiwaną rtęć. Reakcja zachodzi zgodnie z następującym uproszczonym schematem:
2 NaCl(aq) + 2 Hg(l) → 2 NaHg(l) + Cl2(g)
2 NaHg(l) + 2 H2O(l) → 2 NaOH(aq) + H2(g) + 2 Hg(l)
Chociaż metoda rtęciowa pozwala uzyskać bardzo czysty wodorotlenek sodu, ma poważne wady związane z toksycznością rtęci. Rtęć jest niebezpieczna dla środowiska i zdrowia ludzkiego, a jej uwalnianie podczas procesu produkcyjnego stanowiło poważny problem. Z tego powodu metoda ta jest stopniowo wycofywana w wielu krajach.
2. Metoda membranowa
Metoda membranowa jest obecnie najczęściej stosowaną metodą produkcji wodorotlenku sodu. Wykorzystuje specjalne membrany jonowymienne, które selektywnie przepuszczają jony sodu (Na+) z przestrzeni anodowej do przestrzeni katodowej. Dzięki temu zapobiega się mieszaniu roztworu chlorku sodu z powstającym wodorotlenkiem sodu i chlorek sodu nie przedostaje się do produktu końcowego.
Reakcje zachodzące podczas elektrolizy membranowej:
Anoda: 2 Cl-(aq) → Cl2(g) + 2 e-
Katoda: 2 H2O(l) + 2 e- → H2(g) + 2 OH-(aq)
Ogólna reakcja:
2 NaCl(aq) + 2 H2O(l) → 2 NaOH(aq) + Cl2(g) + H2(g)
Zalety metody membranowej:
- Mniejsze zużycie energii w porównaniu z metodą rtęciową.
- Brak użycia rtęci, co eliminuje ryzyko zanieczyszczenia środowiska.
- Produkcja wodorotlenku sodu o wysokiej czystości.
3. Metoda diafragmowa
Metoda diafragmowa wykorzystuje diafragmę azbestową (obecnie coraz częściej zastępowaną materiałami syntetycznymi) do oddzielenia przestrzeni anodowej i katodowej. W wyniku elektrolizy roztworu chlorku sodu powstaje roztwór wodorotlenku sodu zmieszany z niezmienionym chlorkiem sodu. Otrzymany roztwór wymaga dalszego zatężania i oczyszczania, aby uzyskać produkt o odpowiedniej czystości.
Proces jest podobny do metody membranowej, ale diafragma jest bardziej przepuszczalna niż membrana, co powoduje przedostawanie się chlorku sodu do roztworu wodorotlenku.
Zalety metody diafragmowej:
- Niższe koszty inwestycyjne w porównaniu z metodą membranową.
Wady metody diafragmowej:
- Wyższe zużycie energii w porównaniu z metodą membranową.
- Potrzeba dalszego oczyszczania produktu.
- Ryzyko związane z użyciem azbestu (w starszych instalacjach).
Bezpieczeństwo i Środki Ostrożności
Wodorotlenek sodu jest substancją żrącą i należy zachować szczególną ostrożność podczas pracy z nim. Należy zawsze stosować odpowiednie środki ochrony osobistej, takie jak:
- Okulary ochronne: Chronią oczy przed oparzeniami.
- Rękawice ochronne: Zapobiegają uszkodzeniom skóry.
- Fartuch ochronny: Chroni odzież przed zniszczeniem.
W przypadku kontaktu wodorotlenku sodu ze skórą lub oczami, należy natychmiast przemyć je dużą ilością wody i skonsultować się z lekarzem. Należy również unikać wdychania oparów wodorotlenku sodu, ponieważ mogą one powodować podrażnienia dróg oddechowych.
Zastosowania Wodorotlenku Sodu
Wodorotlenek sodu ma bardzo szerokie spektrum zastosowań, między innymi:
- Przemysł chemiczny: Produkcja mydła, detergentów, papieru, sztucznego jedwabiu, barwników, leków, aluminium.
- Przemysł petrochemiczny: Oczyszczanie ropy naftowej.
- Przemysł spożywczy: Czyszczenie urządzeń, regulacja pH.
- Oczyszczanie ścieków: Neutralizacja kwasów, usuwanie metali ciężkich.
- Gospodarstwa domowe: Udrażnianie rur kanalizacyjnych (środki do czyszczenia rur).
Jak widać, wodorotlenek sodu jest niezwykle wszechstronną substancją, bez której trudno wyobrazić sobie współczesny przemysł i życie codzienne. Zrozumienie metod jego otrzymywania i właściwości jest kluczowe dla bezpiecznego i efektywnego wykorzystania tego związku.
Mimo że domowe eksperymenty z produkcją wodorotlenku sodu są generalnie niezalecane z powodu ryzyka i konieczności posiadania specjalistycznego sprzętu, świadomość procesów przemysłowych pozwala lepiej zrozumieć znaczenie tej substancji w naszym świecie. Pamiętajmy o bezpieczeństwie i korzystajmy z wiedzy zawartej w artykule odpowiedzialnie.