Liczba Protonów Neutronów I Elektronów

Witaj! Zastanawiałeś się kiedyś, z czego zbudowany jest świat dookoła nas? Wszystko, dosłownie wszystko, od powietrza, którym oddychasz, po telefon, który trzymasz w ręku, składa się z bardzo małych cząstek, zwanych atomami. A atomy? Atomy składają się z jeszcze mniejszych elementów: protonów, neutronów i elektronów. Spróbujmy przyjrzeć się im bliżej i zrozumieć, czym są, jak się zachowują i dlaczego są tak ważne.
Protony: Dodatni ładunek w sercu atomu
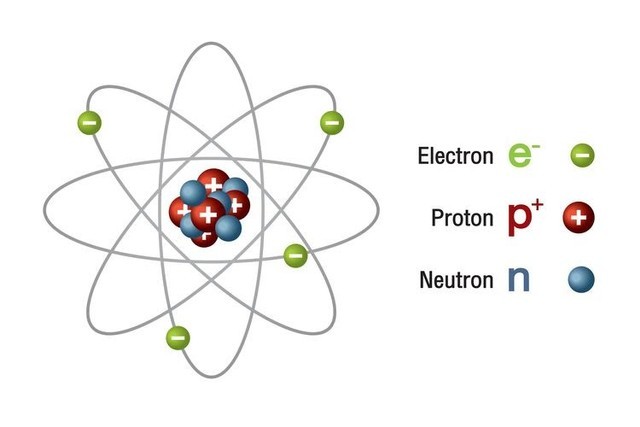
Wyobraź sobie atom jako małe słoneczko. W samym jego centrum, czyli w jądrze atomowym, znajdują się protony. Protony mają ładunek elektryczny dodatni (+). To jakby małe, pozytywne bateryjki w środku atomu. Ilość protonów w jądrze decyduje o tym, jaki to jest pierwiastek. Na przykład, każdy atom wodoru ma jeden proton, a każdy atom węgla ma sześć protonów. To tak, jakby liczba protonów była "numerem identyfikacyjnym" każdego pierwiastka. Zmiana liczby protonów zmienia pierwiastek – to jakby zmienić imię i nazwisko osoby, czyniąc ją kimś innym!
Dla wizualnych: Wyobraź sobie atom wodoru – to kółko (jądro) z jednym (+) w środku i kropka krążąca dookoła (elektron – o nim za chwilę). Atom węgla to z kolei kółko z sześcioma (+) w środku i sześcioma kropkami krążącymi dookoła.
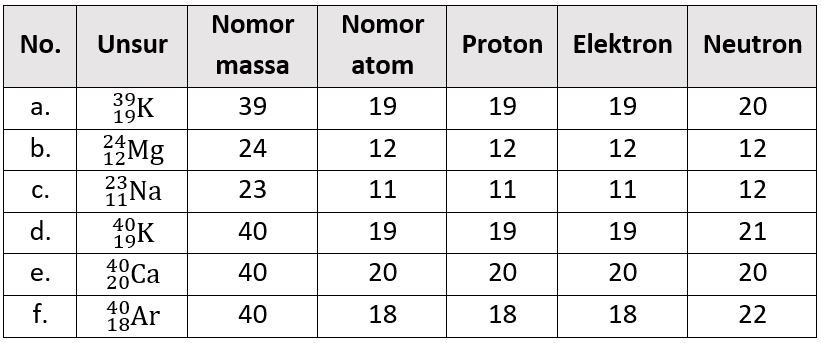
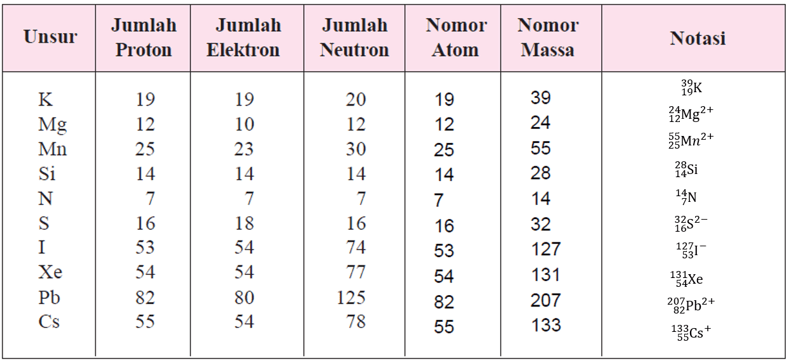
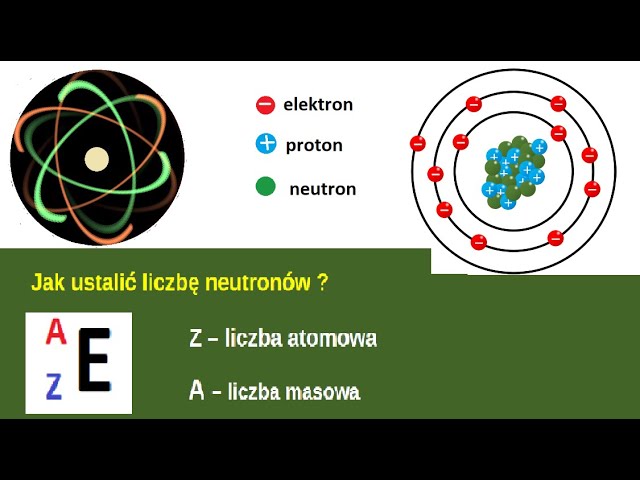
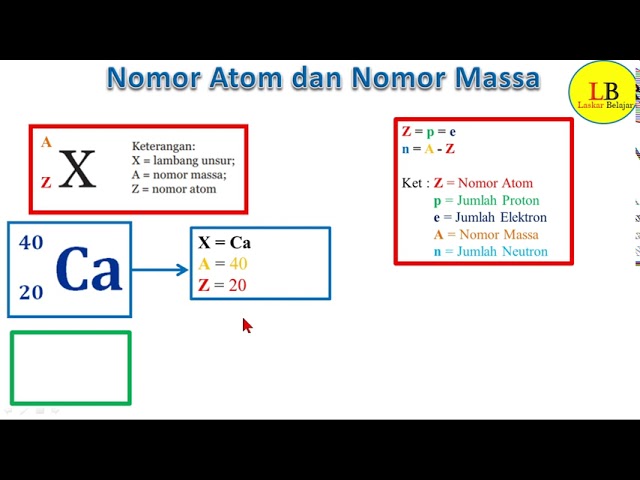
Liczba protonów w jądrze atomowym nazywana jest liczbą atomową. Oznacza się ją literą Z. Spójrz na układ okresowy pierwiastków – każdy pierwiastek ma przypisaną liczbę atomową. To właśnie ta liczba mówi nam, ile protonów znajduje się w jądrze atomu danego pierwiastka.
Neutrony: Neutralni towarzysze protonów
Oprócz protonów, w jądrze atomowym znajdują się również neutrony. Neutrony, jak sama nazwa wskazuje, są elektrycznie obojętne. Nie mają ładunku (+ ani -). Można je sobie wyobrazić jako neutralnych towarzyszy protonów, pomagających utrzymać stabilność jądra atomowego. Funkcją neutronów jest amortyzacja sił odpychania, które występują między protonami, ponieważ protony o tym samym ładunku dodatnim odpychają się nawzajem.
Ilość neutronów w jądrze atomu danego pierwiastka może się różnić. Atomy tego samego pierwiastka, które różnią się liczbą neutronów, nazywamy izotopami. Na przykład, węgiel-12 ma 6 protonów i 6 neutronów, a węgiel-14 ma 6 protonów i 8 neutronów. Oba to węgiel, ale różnią się masą.
Dla wizualnych: Wyobraź sobie jądro atomowe jako salę zabaw. Protony to energiczne dzieciaki, które chcą się nawzajem odpychać (bo mają ten sam ładunek). Neutrony to opiekunki, które je uspokajają i zapobiegają chaosowi, utrzymując wszystko w kupie.
Elektrony: Wirujące chmury ujemnego ładunku
Wokół jądra atomowego krążą elektrony. Elektrony mają ładunek elektryczny ujemny (-). Krążą one po tak zwanych orbitalach, tworząc coś w rodzaju "chmury" elektronowej wokół jądra. Liczba elektronów w atomie zazwyczaj jest równa liczbie protonów, co sprawia, że atom jako całość jest elektrycznie obojętny.
Wyobraź sobie elektrony jako planety krążące wokół słońca (jądra atomowego). Każda planeta krąży po swojej orbicie. Podobnie elektrony krążą wokół jądra po różnych orbitalach. Niektóre orbity są bliżej jądra, inne dalej. Im bliżej orbita jądra, tym mniej energii elektron potrzebuje, aby na niej pozostać.
Elektrony odgrywają kluczową rolę w tworzeniu wiązań chemicznych. To właśnie elektrony "łączą" atomy ze sobą, tworząc cząsteczki. Na przykład, dwa atomy wodoru łączą się ze sobą, tworząc cząsteczkę wodoru (H2), a dwa atomy wodoru i jeden atom tlenu łączą się ze sobą, tworząc cząsteczkę wody (H2O). To właśnie wymiana i współdzielenie elektronów między atomami umożliwia istnienie wszelkiego rodzaju związków chemicznych.
Dla wizualnych: Wyobraź sobie dwa magnesy. Magnesy z różnymi biegunami (plus i minus) przyciągają się. Podobnie elektrony (minus) są przyciągane do protonów (plus) w jądrze atomowym.
Podsumowanie: Protony, Neutrony, Elektrony w działaniu
Podsumowując:
- Protony: Mają ładunek dodatni (+), znajdują się w jądrze atomowym, a ich liczba decyduje o tym, jaki to pierwiastek.
- Neutrony: Są elektrycznie obojętne, znajdują się w jądrze atomowym i pomagają utrzymać jego stabilność.
- Elektrony: Mają ładunek ujemny (-), krążą wokół jądra atomowego i odpowiadają za tworzenie wiązań chemicznych.
Ilość protonów, neutronów i elektronów w atomie determinuje jego właściwości chemiczne i fizyczne. To, jak te cząstki oddziałują ze sobą, wpływa na to, jak dany pierwiastek zachowuje się w różnych sytuacjach, jak łączy się z innymi pierwiastkami i jakie tworzy związki. Zrozumienie roli protonów, neutronów i elektronów jest kluczowe do zrozumienia chemii i fizyki.
Pamiętaj, świat jest zbudowany z atomów, a atomy z protonów, neutronów i elektronów. To fascynujące, prawda?