Liczba Powłok Elektronowych Jak Obliczyć

Zrozumienie struktury atomu jest fundamentalne dla chemii i fizyki. Jednym z kluczowych aspektów tej struktury jest liczba powłok elektronowych. Powłoki elektronowe, zwane również poziomami energetycznymi, opisują obszary wokół jądra atomowego, w których najprawdopodobniej znajdują się elektrony. Zrozumienie, jak obliczyć i interpretować liczbę powłok elektronowych, pozwala na przewidywanie właściwości chemicznych pierwiastków i ich zdolności do tworzenia wiązań.
Podstawowe Pojęcia dotyczące Powłok Elektronowych
Elektrony nie krążą wokół jądra atomowego w sposób chaotyczny. Zajmują one określone poziomy energetyczne, które nazywamy powłokami elektronowymi. Każda powłoka może pomieścić maksymalną, określoną liczbę elektronów. Koncepcja ta została wprowadzona przez Nielsa Bohra w jego modelu atomu, choć współczesny model kwantowy oferuje bardziej precyzyjny opis.
Kwantowe Numery
Opis stanu elektronu w atomie wymaga użycia czterech liczb kwantowych. Najważniejsza z punktu widzenia powłok jest główna liczba kwantowa (n). Przyjmuje ona wartości całkowite, zaczynając od 1 (n=1, 2, 3, ...). Główna liczba kwantowa bezpośrednio odpowiada numerowi powłoki elektronowej. Powłoka z n=1 to pierwsza powłoka, n=2 to druga powłoka, i tak dalej.
Dla danej wartości n, istnieją również podpowłoki, opisane przez poboczną liczbę kwantową (l). Wartości l wahają się od 0 do n-1. Dla n=1, l może być tylko 0. Dla n=2, l może być 0 lub 1. Te podpowłoki są często oznaczane literami: l=0 to podpowłoka *s*, l=1 to *p*, l=2 to *d*, l=3 to *f*, i tak dalej.
Maksymalna Liczba Elektronów na Powłoce
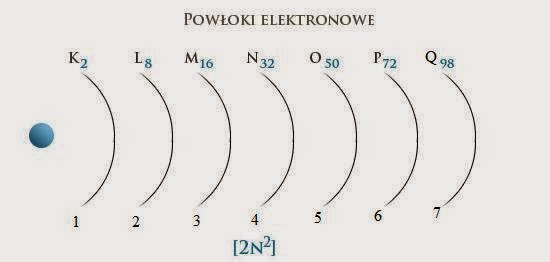
Maksymalną liczbę elektronów, którą może pomieścić dana powłoka, oblicza się ze wzoru: 2n2, gdzie n to numer powłoki.
- n=1: 2 * 12 = 2 elektrony
- n=2: 2 * 22 = 8 elektronów
- n=3: 2 * 32 = 18 elektronów
- n=4: 2 * 42 = 32 elektrony
Warto zauważyć, że dla pierwiastków o wyższych numerach atomowych, reguła ta nie zawsze jest ściśle przestrzegana w kolejności zapełniania powłok (patrz Reguła Madelunga).
Jak Obliczyć Liczbę Powłok Elektronowych Pierwiastka
Najprostszym sposobem na określenie liczby powłok elektronowych pierwiastka jest znalezienie jego położenia w układzie okresowym pierwiastków. Numer okresu, w którym znajduje się pierwiastek, odpowiada liczbie powłok elektronowych w jego atomie.
Krok po Kroku:
- Znajdź pierwiastek w układzie okresowym.
- Zidentyfikuj numer okresu, w którym się znajduje. Numer okresu to numer rzędu poziomego w układzie okresowym.
- Numer okresu to liczba powłok elektronowych.
Przykłady:
- Wodór (H): Znajduje się w pierwszym okresie, więc ma 1 powłokę elektronową.
- Tlen (O): Znajduje się w drugim okresie, więc ma 2 powłoki elektronowe.
- Sód (Na): Znajduje się w trzecim okresie, więc ma 3 powłoki elektronowe.
- Żelazo (Fe): Znajduje się w czwartym okresie, więc ma 4 powłoki elektronowe.
Alternatywnie, można określić konfigurację elektronową pierwiastka, która wskazuje rozmieszczenie elektronów na poszczególnych powłokach i podpowłokach. Najwyższy numer powłoki w konfiguracji elektronowej wskazuje liczbę powłok elektronowych.
Na przykład, konfiguracja elektronowa sodu (Na) to 1s2 2s2 2p6 3s1. Najwyższy numer powłoki to 3, więc sód ma 3 powłoki elektronowe.
Reguła Madelunga (n+l)
Kolejność zapełniania powłok elektronowych nie zawsze jest intuicyjna. Reguła Madelunga, znana również jako reguła (n+l), pomaga przewidzieć kolejność zapełniania podpowłok. Reguła ta mówi, że podpowłoki są zapełniane w kolejności rosnącej sumy głównej liczby kwantowej (n) i pobocznej liczby kwantowej (l). Jeśli dwie podpowłoki mają taką samą sumę (n+l), najpierw zapełniana jest podpowłoka z niższym n.
Na przykład, 4s (n=4, l=0, n+l=4) zapełniana jest przed 3d (n=3, l=2, n+l=5), mimo że intuicyjnie mogłoby się wydawać, że 3d powinno być zapełniane wcześniej.
Ta reguła jest bardzo przydatna do przewidywania konfiguracji elektronowych i zrozumienia, dlaczego niektóre pierwiastki zachowują się w sposób, który wydaje się być sprzeczny z prostą regułą 2n2.
Znaczenie Liczby Powłok Elektronowych
Liczba powłok elektronowych ma istotny wpływ na właściwości chemiczne pierwiastka.
- Wielkość atomu: Im więcej powłok elektronowych, tym większy jest atom. Elektrony na bardziej zewnętrznych powłokach znajdują się dalej od jądra.
- Energia jonizacji: Energia jonizacji to energia potrzebna do oderwania elektronu od atomu. Pierwiastki z większą liczbą powłok elektronowych mają zwykle niższą energię jonizacji, ponieważ zewnętrzne elektrony są słabiej przyciągane przez jądro.
- Elektroujemność: Elektroujemność to miara zdolności atomu do przyciągania elektronów w wiązaniu chemicznym. Pierwiastki z mniejszą liczbą powłok elektronowych mają zwykle wyższą elektroujemność.
- Reaktywność chemiczna: Liczba elektronów walencyjnych (elektronów na najbardziej zewnętrznej powłoce) determinuje sposób, w jaki pierwiastek będzie reagował z innymi pierwiastkami. Liczba powłok wpływa na dostępność tych elektronów walencyjnych do tworzenia wiązań.
Przykłady Real-World: Zastosowania w Chemii i Materiałoznawstwie
Zrozumienie liczby powłok elektronowych i konfiguracji elektronowych jest kluczowe w wielu dziedzinach nauki i technologii.
- Projektowanie nowych materiałów: Wiedza o właściwościach elektronowych pierwiastków pozwala na tworzenie materiałów o pożądanych cechach, np. w elektronice, gdzie kluczowe są półprzewodniki. Krzem (Si), który znajduje się w trzecim okresie i ma 3 powłoki elektronowe, jest podstawowym materiałem półprzewodnikowym. Doping krzemu innymi pierwiastkami (np. fosforem lub borem) modyfikuje jego właściwości elektryczne, a zrozumienie ich konfiguracji elektronowej pozwala na precyzyjne kontrolowanie tego procesu.
- Kataliza: Wiele kataliz działa poprzez absorpcję cząsteczek na powierzchni metalu. Właściwości elektronowe metalu, w tym liczba powłok elektronowych i konfiguracja elektronowa, wpływają na jego zdolność do absorpcji i aktywacji tych cząsteczek. Przykładowo, platyna (Pt) jest szeroko stosowana jako katalizator w przemyśle chemicznym ze względu na jej specyficzne właściwości elektronowe.
- Projektowanie leków: Oddziaływania między lekiem a jego celem biologicznym (np. białkiem) zależą od właściwości chemicznych obu cząsteczek. Zrozumienie struktury elektronowej atomów wchodzących w skład leku i białka pozwala na projektowanie leków, które będą silniej i bardziej selektywnie wiązać się z celem.
- Analiza spektroskopowa: Techniki spektroskopowe, takie jak spektroskopia absorpcyjna i emisyjna, wykorzystują interakcję światła z materią do identyfikacji i charakterystyki substancji. Energia, przy której zachodzi absorpcja lub emisja światła, zależy od struktury elektronowej atomów i jonów, w tym od liczby powłok elektronowych i różnic energii między nimi.
Na przykład, obserwując widmo emisyjne gazów rozgrzanych w rurce wyładowczej, możemy zidentyfikować pierwiastki obecne w gazie. Każdy pierwiastek ma unikalny zestaw linii widmowych, odpowiadających przejściom elektronów między różnymi poziomami energetycznymi. Analizując położenie tych linii widmowych, możemy określić strukturę elektronową atomu i liczbę jego powłok elektronowych.
Podsumowanie
Liczba powłok elektronowych jest fundamentalnym pojęciem w chemii i fizyce, które pozwala na zrozumienie struktury atomu i przewidywanie właściwości chemicznych pierwiastków. Można ją łatwo określić, znajdując pierwiastek w układzie okresowym i odczytując numer okresu. Znajomość tego parametru jest kluczowa w wielu dziedzinach nauki i technologii, od projektowania nowych materiałów po rozwój leków.
Zachęcamy do dalszego zgłębiania wiedzy o strukturze atomu i jego wpływie na świat wokół nas! Spróbuj samodzielnie określić liczbę powłok elektronowych dla różnych pierwiastków w układzie okresowym i zastanów się, jak ta liczba wpływa na ich właściwości.