Kwasy Tlenowe I Beztlenowe Wzory
Chemia bywa postrzegana jako przedmiot pełen skomplikowanych wzorów i abstrakcyjnych koncepcji. Wielu uczniów, a nawet osób dorosłych, odczuwa trudności w zrozumieniu i zapamiętaniu różnic między kwasami tlenowymi i beztlenowymi. Ten artykuł ma na celu rozjaśnić te pojęcia, pokazując, jak wpływają one na nasze codzienne życie i oferując praktyczne wskazówki do ich zapamiętania.
Czy kiedykolwiek zastanawiałeś się, co powoduje kwaśny smak cytryny, albo dlaczego niektóre środki czyszczące są tak skuteczne? Kluczem są właśnie kwasy, a różnica między tlenowymi i beztlenowymi ma fundamentalne znaczenie dla zrozumienia ich właściwości i zastosowań.
Kwasy – Podstawowe informacje
Zacznijmy od podstaw. Kwasy to substancje, które w roztworze wodnym uwalniają jony wodorowe (H+). To właśnie obecność tych jonów nadaje kwasom charakterystyczny kwaśny smak (choć absolutnie nie wolno próbować kwasów w laboratorium!). Kwasy reagują z metalami, tworząc sole, i neutralizują zasady.
Podział kwasów
Kwasy dzielimy na wiele grup, ale najważniejszy podział dla naszych celów to podział na:
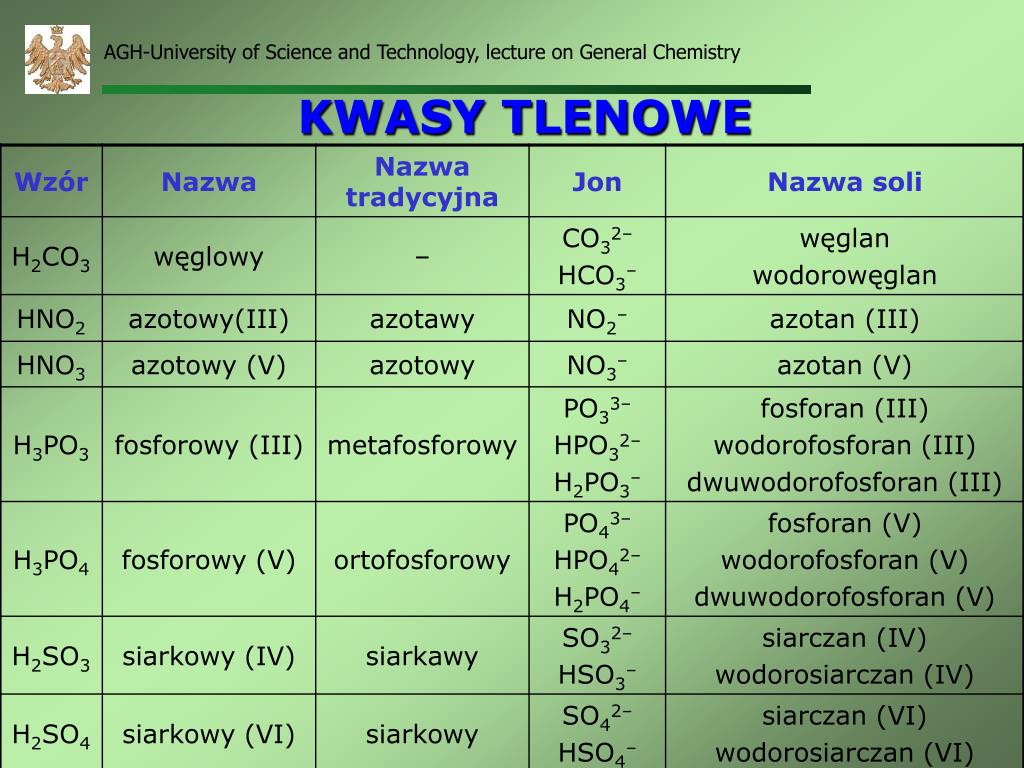
- Kwasy tlenowe: Zawierają w swojej cząsteczce atomy tlenu, oprócz wodoru i innego niemetalu.
- Kwasy beztlenowe: Nie zawierają atomów tlenu. Składają się jedynie z wodoru i niemetalu.
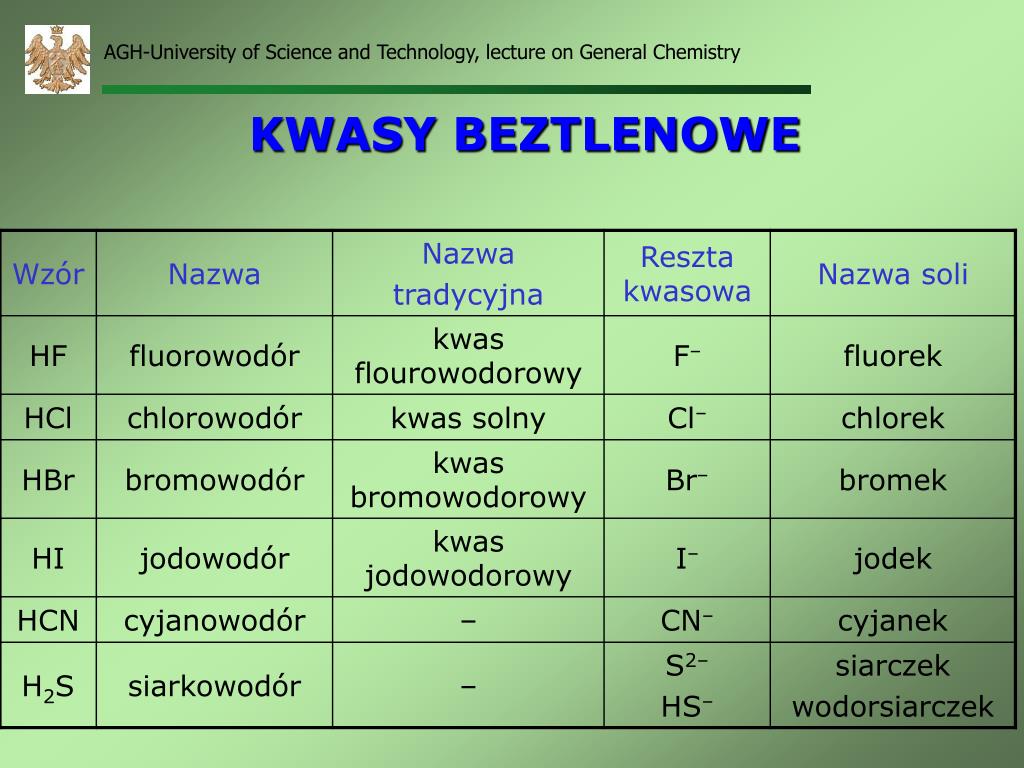
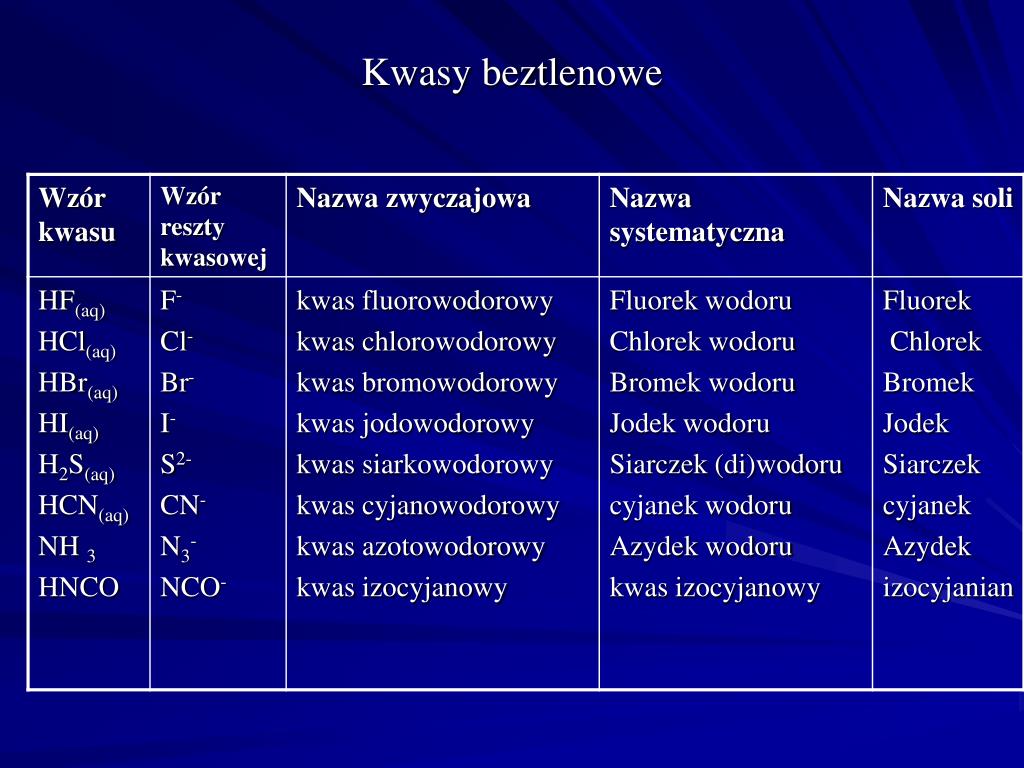
Kwasy Beztlenowe – Prosta budowa i silne właściwości
Kwasy beztlenowe, jak sama nazwa wskazuje, w swojej strukturze nie zawierają atomów tlenu. Są to połączenia wodoru (H) z jednym z halogenów (fluor - F, chlor - Cl, brom - Br, jod - I) lub siarką (S). Ogólny wzór kwasu beztlenowego to HX, gdzie X to atom niemetalu.
Przykłady kwasów beztlenowych:
- Kwas chlorowodorowy (HCl): Znany również jako kwas solny, jest bardzo silnym kwasem, używanym w przemyśle (np. do trawienia metali), w laboratoriach oraz w żołądku do trawienia pokarmów.
- Kwas fluorowodorowy (HF): Wyjątkowo żrący, używany do trawienia szkła. Należy zachować szczególną ostrożność przy pracy z nim.
- Kwas bromowodorowy (HBr): Używany w syntezie organicznej i do produkcji niektórych leków.
- Kwas jodowodorowy (HI): Najsilniejszy kwas halogenowodorowy, silny reduktor.
- Kwas siarkowodorowy (H2S): Charakteryzuje się zapachem zgniłych jaj. Jest bardzo toksyczny i występuje w kanalizacji i w gazach wulkanicznych.
Wpływ na życie: Kwas solny (HCl) jest produkowany przez komórki okładzinowe w żołądku i odgrywa kluczową rolę w trawieniu białek. Jego obecność w odpowiednim stężeniu jest niezbędna do prawidłowego funkcjonowania układu pokarmowego. Zaburzenia w produkcji kwasu solnego mogą prowadzić do problemów trawiennych.
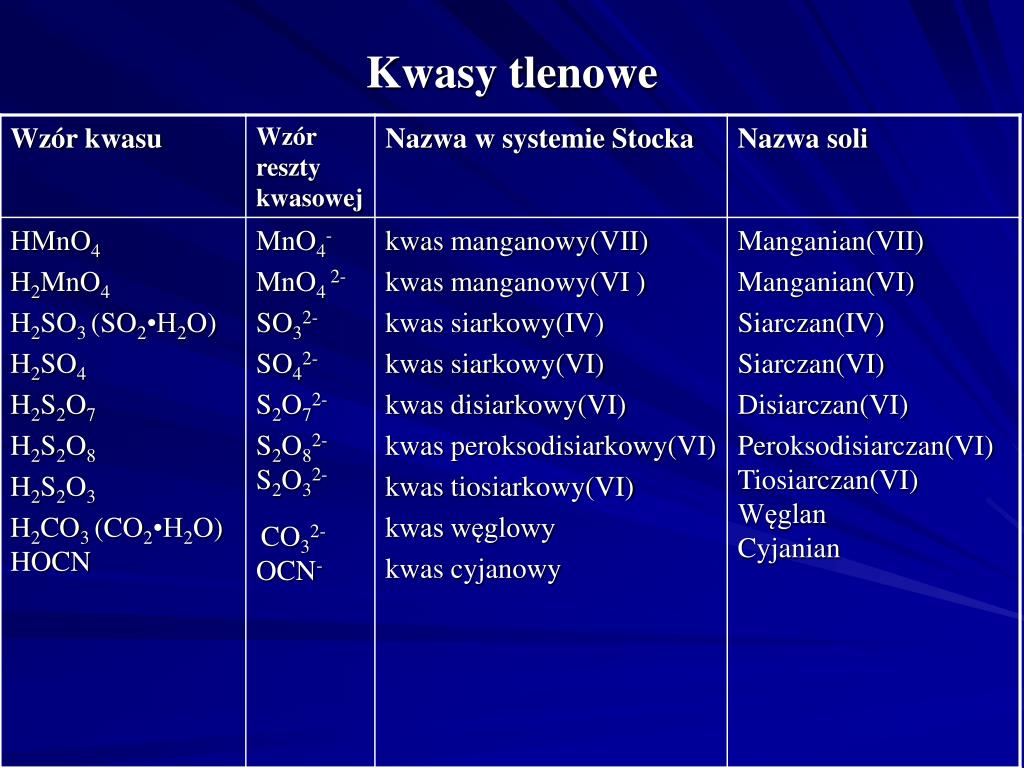
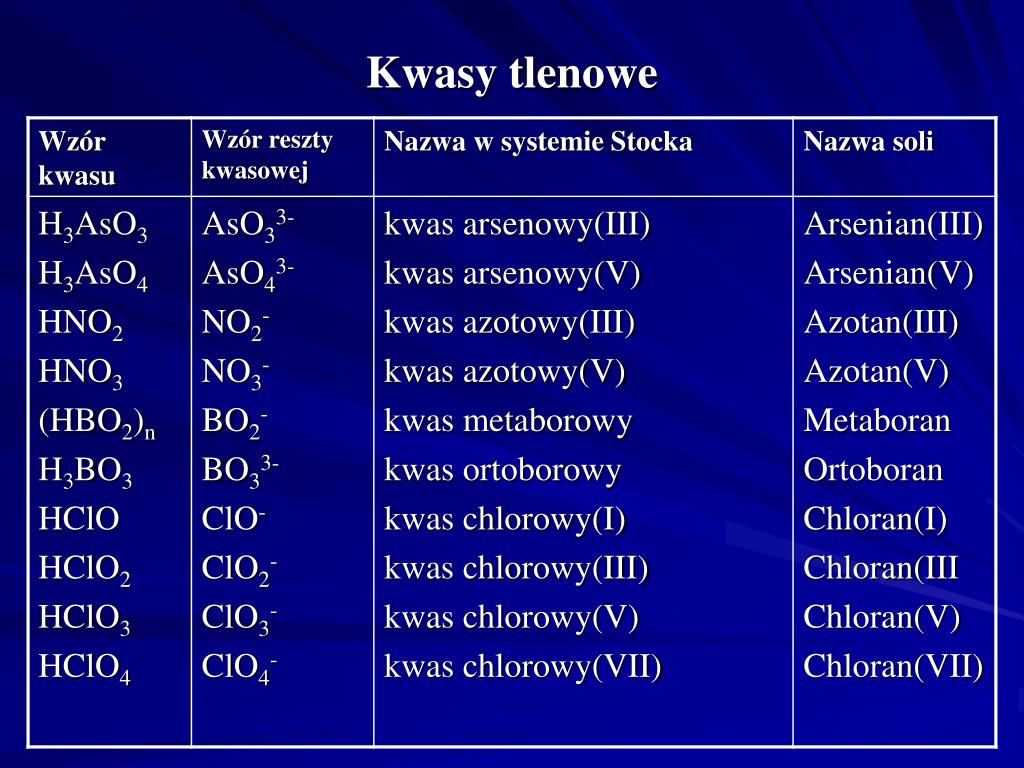
Kwasy Tlenowe – Złożona struktura i różnorodne zastosowania
Kwasy tlenowe, w odróżnieniu od beztlenowych, zawierają w swojej strukturze atomy tlenu. Ich budowa jest bardziej skomplikowana, a właściwości – bardziej zróżnicowane. Ogólny wzór kwasu tlenowego to HxXOy, gdzie X to atom niemetalu, a x i y to liczby atomów wodoru i tlenu, odpowiednio.
Przykłady kwasów tlenowych:
- Kwas siarkowy (VI) (H2SO4): Jeden z najważniejszych kwasów w przemyśle. Używany do produkcji nawozów, detergentów, farb, tworzyw sztucznych i wielu innych produktów. Jest silnie żrący i higroskopijny.
- Kwas azotowy (V) (HNO3): Używany do produkcji nawozów sztucznych, materiałów wybuchowych, barwników. Jest silnym utleniaczem.
- Kwas fosforowy (V) (H3PO4): Używany w produkcji nawozów, detergentów, środków czyszczących, a także w przemyśle spożywczym (dodatek do napojów).
- Kwas węglowy (H2CO3): Powstaje w wyniku rozpuszczania dwutlenku węgla (CO2) w wodzie. Jest słabym kwasem, obecnym w napojach gazowanych i odgrywającym ważną rolę w regulacji pH krwi.
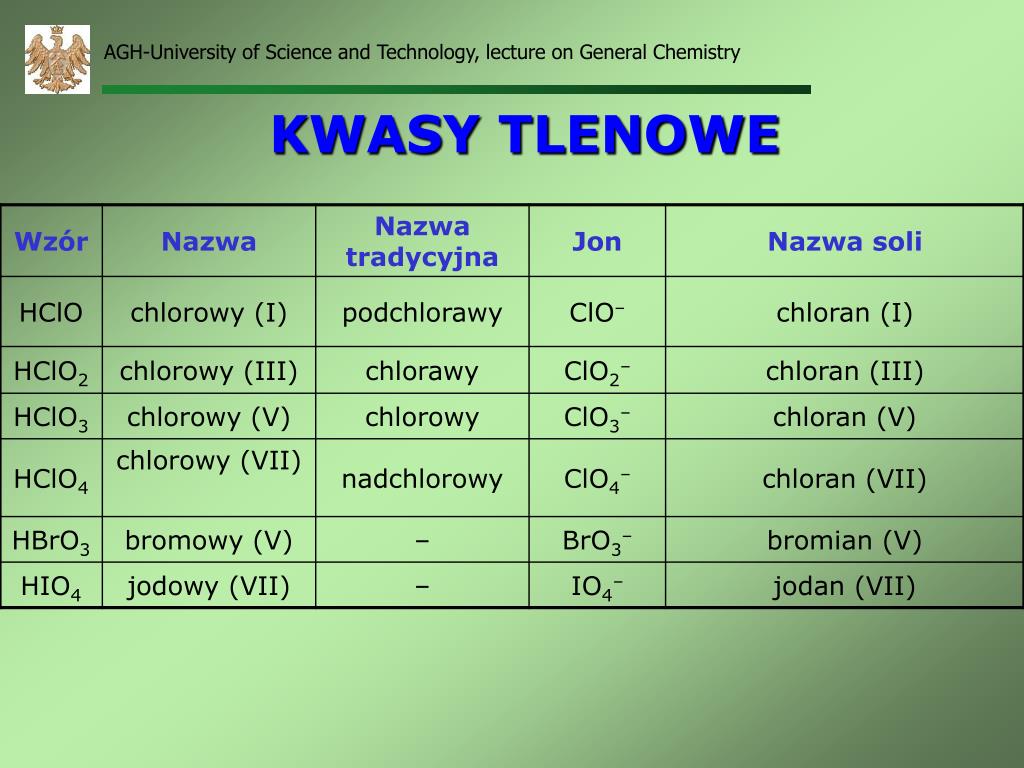
- Kwas chlorowy (I) (HClO): Słaby kwas, składnik środków dezynfekujących i wybielających.
Wpływ na życie: Kwas węglowy (H2CO3) odgrywa kluczową rolę w regulacji pH krwi. Jest częścią układu buforowego, który pomaga utrzymać stałe pH, niezbędne do prawidłowego funkcjonowania organizmu. Zaburzenia w tym układzie mogą prowadzić do poważnych problemów zdrowotnych. Ponadto, kwas fosforowy (V) (H3PO4) jest składnikiem nawozów, które umożliwiają wzrost roślin i produkcję żywności.
Porównanie kwasów tlenowych i beztlenowych
Kluczową różnicą między kwasami tlenowymi i beztlenowymi jest obecność tlenu w ich strukturze. Ta różnica wpływa na ich właściwości, siłę i zastosowania.
| Cecha | Kwas Beztlenowy | Kwas Tlenowy |
|---|---|---|
| Obecność tlenu | Brak | Obecny |
| Struktura | Prosta (HX) | Złożona (HxXOy) |
| Przykłady | HCl, HF, HBr, HI, H2S | H2SO4, HNO3, H3PO4, H2CO3, HClO |
| Zastosowania | Trawienie metali, synteza organiczna, trawienie pokarmów (HCl w żołądku) | Produkcja nawozów, detergentów, materiałów wybuchowych, napojów gazowanych |
Jak zapamiętać wzory kwasów?
Zapamiętanie wzorów kwasów może wydawać się trudne, ale istnieje kilka skutecznych strategii:
- Zrozumienie budowy: Zamiast uczyć się na pamięć, spróbuj zrozumieć, jak zbudowane są kwasy tlenowe i beztlenowe. Zwróć uwagę na obecność tlenu i jego wpływ na wzór.
- Kojarzenie: Twórz skojarzenia między nazwą kwasu a jego wzorem. Na przykład, "siarkowy" kojarzy się z siarką (S), a "azotowy" z azotem (N).
- Powtarzanie: Regularnie powtarzaj wzory kwasów. Możesz użyć kartki z notatkami, aplikacji mobilnych lub quizów online.
- Używanie: Staraj się używać wzorów kwasów w praktyce. Pisząc reakcje chemiczne lub rozwiązując zadania, utrwalisz je w pamięci.
- Grupy funkcyjne: Zauważ, że niektóre kwasy tlenowe mają podobne grupy funkcyjne. Na przykład, kwasy siarkowe, azotowe i fosforowe mają atomy tlenu połączone z centralnym atomem niemetalu.
Potencjalne problemy i kontrargumenty
Niektórzy mogą twierdzić, że zapamiętywanie wzorów kwasów jest bezcelowe, ponieważ dostęp do informacji jest teraz tak łatwy. Jednak zrozumienie struktury i właściwości kwasów jest kluczowe dla zrozumienia wielu procesów chemicznych i biologicznych. Zapamiętanie podstawowych wzorów ułatwia zrozumienie bardziej zaawansowanych koncepcji.
Innym kontrargumentem może być to, że kwasy są niebezpieczne i nie warto się nimi zajmować. To prawda, że niektóre kwasy są bardzo żrące i wymagają ostrożnego obchodzenia się z nimi. Jednak kwasy odgrywają niezwykle ważną rolę w naszym życiu, od trawienia pokarmów po produkcję żywności i leków. Zrozumienie ich właściwości pozwala na bezpieczne i skuteczne wykorzystanie ich w różnych dziedzinach.
Podsumowanie i wnioski
Rozróżnienie między kwasami tlenowymi i beztlenowymi jest fundamentalne dla zrozumienia chemii. Kwasy beztlenowe, proste w budowie, ale często bardzo silne, znajdują zastosowanie w przemyśle i w procesach biologicznych. Kwasy tlenowe, bardziej złożone, odgrywają kluczową rolę w produkcji nawozów, detergentów i wielu innych produktów.
Pamiętaj, że nauka chemii to proces. Nie zrażaj się trudnościami i regularnie powtarzaj materiał. Zrozumienie budowy i właściwości kwasów pozwoli Ci lepiej zrozumieć świat wokół Ciebie.
Czy ten artykuł pomógł Ci zrozumieć różnicę między kwasami tlenowymi i beztlenowymi? Jakie inne tematy z chemii chciałbyś, abyśmy poruszyli?