Kartkówka Alkohole Chemia Klasa 8

Hej ósmoklasisto! Zbliża się kartkówka z alkoholi w ramach chemii? Nie panikuj! Ten artykuł jest stworzony specjalnie dla Ciebie, aby pomóc Ci zrozumieć kluczowe zagadnienia i skutecznie przygotować się do tego wyzwania. Razem przejdziemy przez najważniejsze informacje, tak abyś na kartkówce mógł/mogła zabłysnąć wiedzą. Zapomnij o stresie – zrozumienie to klucz do sukcesu!
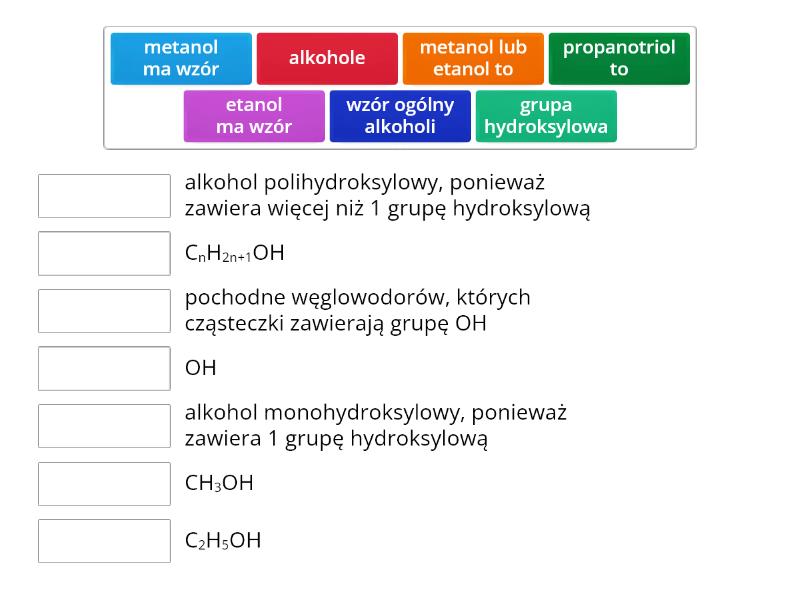
Czym są Alkohole? Krótka Definicja
Zacznijmy od podstaw. Alkohole to organiczne związki chemiczne, w których cząsteczce znajduje się grupa hydroksylowa (-OH), przyłączona do atomu węgla. Brzmi skomplikowanie? Spokojnie! Wyobraź sobie, że do łańcucha węglowego (czyli szkieletu cząsteczki organicznej) doklejona jest "rączka" -OH. Ta rączka nadaje alkoholom ich charakterystyczne właściwości.
Klasyfikacja Alkoholi
Alkohole możemy podzielić na różne grupy w zależności od kilku kryteriów:
- Liczba grup -OH:
- Monoalkohole: Zawierają jedną grupę -OH (np. etanol, metanol). Są to najczęściej spotykane alkohole.
- Polialkohole: Zawierają więcej niż jedną grupę -OH (np. glicerol, glikol etylenowy). Posiadają silniejsze właściwości higroskopijne.
- Rzędowość atomu węgla, do którego przyłączona jest grupa -OH:
- Alkohole pierwszorzędowe: Grupa -OH przyłączona do atomu węgla związanego z jednym innym atomem węgla.
- Alkohole drugorzędowe: Grupa -OH przyłączona do atomu węgla związanego z dwoma innymi atomami węgla.
- Alkohole trzeciorzędowe: Grupa -OH przyłączona do atomu węgla związanego z trzema innymi atomami węgla.
Właściwości Alkoholi – Co Musisz Wiedzieć?
Właściwości alkoholi zależą od długości łańcucha węglowego i obecności grupy hydroksylowej. Oto kilka kluczowych aspektów:
- Stan skupienia:
- Krótkołańcuchowe alkohole (np. metanol, etanol) są cieczami o charakterystycznym zapachu.
- Wraz ze wzrostem długości łańcucha węglowego, alkohole stają się bardziej oleiste i mniej lotne.
- Rozpuszczalność w wodzie:
- Krótkołańcuchowe alkohole dobrze rozpuszczają się w wodzie dzięki tworzeniu wiązań wodorowych z cząsteczkami wody. Grupa -OH jest hydrofilowa (lubi wodę).
- Wraz ze wzrostem długości łańcucha węglowego, rozpuszczalność w wodzie maleje, ponieważ część hydrofobowa (nielubiąca wody) staje się dominująca.
- Temperatura wrzenia:
- Alkohole mają wyższe temperatury wrzenia niż odpowiadające im alkany (węglowodory) o podobnej masie cząsteczkowej. Wynika to z obecności wiązań wodorowych między cząsteczkami alkoholi.
- Toksyczność:
- Nie wszystkie alkohole są bezpieczne! Metanol jest silnie trujący, nawet w małych ilościach, i może powodować ślepotę, a nawet śmierć. Etanol, czyli alkohol spożywczy, również w nadmiarze jest szkodliwy dla zdrowia.
Najważniejsze Alkohole – Poznaj Ich Bliżej
Teraz przyjrzyjmy się kilku najważniejszym alkoholom, które najprawdopodobniej pojawią się na Twojej kartkówce:
Metanol (CH3OH)
- Znany również jako alkohol metylowy.
- Silnie trujący! Nie nadaje się do spożycia.
- Stosowany jako rozpuszczalnik, dodatek do paliw oraz w produkcji formaldehydu.
- Charakteryzuje się podobnym zapachem do etanolu, co zwiększa ryzyko pomyłki.
Etanol (C2H5OH)
- Znany również jako alkohol etylowy.
- Alkohol spożywczy, obecny w napojach alkoholowych (oczywiście, w odpowiednich ilościach!).
- Stosowany jako rozpuszczalnik, środek dezynfekujący oraz w produkcji kosmetyków i leków.
- Otrzymywany głównie w procesie fermentacji cukrów lub syntetycznie z etenu.
Glicerol (C3H5(OH)3)
- Polialkohol (zawiera trzy grupy -OH).
- Bezbarwna, gęsta ciecz o słodkim smaku.
- Ma silne właściwości higroskopijne (pochłania wodę z otoczenia).
- Stosowany w kosmetykach (jako składnik nawilżający), farmacji (jako składnik maści i syropów) oraz w produkcji materiałów wybuchowych (np. nitrogliceryny).
Glikol Etylenowy (C2H4(OH)2)
- Polialkohol (zawiera dwie grupy -OH).
- Bezbarwna, oleista ciecz.
- Toksyczny!
- Stosowany jako składnik płynów chłodniczych w samochodach (obniża temperaturę zamarzania wody) oraz w produkcji tworzyw sztucznych.
Reakcje Alkoholi – Co Reaguje z Alkoholami?
Zrozumienie reakcji chemicznych, w których biorą udział alkohole, jest kluczowe. Oto kilka przykładów:
- Spalanie: Alkohole ulegają spalaniu, tworząc dwutlenek węgla i wodę.
- Całkowite spalanie: C2H5OH + 3O2 → 2CO2 + 3H2O
- Niecałkowite spalanie (przy niedoborze tlenu): Może prowadzić do powstania tlenku węgla (CO) – bardzo trującego gazu – lub sadzy.
- Reakcje z metalami aktywnymi: Alkohole reagują z metalami aktywnymi (np. sód, potas), tworząc alkoholany i wydzielając wodór.
- C2H5OH + Na → C2H5ONa + ½ H2
- Estryfikacja: Alkohole reagują z kwasami karboksylowymi, tworząc estry i wodę. Jest to reakcja odwracalna i wymaga obecności katalizatora (np. kwasu siarkowego).
- C2H5OH + CH3COOH → CH3COOC2H5 + H2O (w obecności H2SO4)
- Odwadnianie: W obecności katalizatora (np. kwasu siarkowego lub tlenku glinu) alkohole mogą ulegać odwadnianiu, prowadząc do powstania alkenów lub eterów.
- C2H5OH → C2H4 + H2O (w obecności H2SO4, wysoka temperatura) - Powstaje eten.
Jak Skutecznie Przygotować się do Kartkówki?
Oto kilka praktycznych wskazówek, które pomogą Ci zdać kartkówkę z alkoholi na piątkę (lub szóstkę!):
- Powtórz podstawowe definicje: Upewnij się, że rozumiesz, czym są alkohole, jaka jest grupa funkcyjna, i jak je klasyfikować.
- Zapamiętaj wzory i nazwy: Naucz się wzorów strukturalnych i nazw najważniejszych alkoholi (metanol, etanol, glicerol, glikol etylenowy).
- Zrozum właściwości: Przemyśl, dlaczego alkohole mają takie, a nie inne właściwości (rozpuszczalność, temperatura wrzenia, toksyczność).
- Przeanalizuj reakcje: Naucz się pisać równania reakcji chemicznych, w których biorą udział alkohole. Zwróć uwagę na warunki reakcji i produkty.
- Rozwiąż zadania: Wykorzystaj podręcznik, zeszyt ćwiczeń i internet do znalezienia zadań dotyczących alkoholi. Rozwiązywanie zadań to najlepszy sposób na utrwalenie wiedzy.
- Ucz się aktywnie: Nie tylko czytaj notatki! Twórz mapy myśli, rysuj schematy, tłumacz zagadnienia własnymi słowami.
- Zapytaj, jeśli czegoś nie rozumiesz: Nie wstydź się pytać nauczyciela lub kolegów z klasy, jeśli masz jakieś wątpliwości.
- Zadbaj o sen i odpoczynek: Wyspany i wypoczęty umysł lepiej przyswaja wiedzę. Nie zostawiaj nauki na ostatnią chwilę!
Podsumowanie – Wiedza To Potęga!
Kartkówka z alkoholi wcale nie musi być straszna! Z odpowiednim przygotowaniem i pozytywnym nastawieniem możesz osiągnąć sukces. Pamiętaj, że zrozumienie jest ważniejsze niż zapamiętywanie. Staraj się zrozumieć, dlaczego alkohole mają takie właściwości i jak reagują z innymi substancjami. Wykorzystaj ten artykuł jako punkt wyjścia do dalszej nauki i eksploracji fascynującego świata chemii. Powodzenia na kartkówce!