Jak Odróżnić Alkohole Monohydroksylowe Od Polihydroksylowych

Okej, porozmawiajmy o tym, jak odróżnić alkohole monohydroksylowe od polihydroksylowych! To wcale nie jest takie trudne, jak mogłoby się wydawać. Najważniejsze, to zrozumieć, co oznaczają te nazwy.
Alkohol, to w chemii organicznej związek, który ma w swojej strukturze grupę hydroksylową (-OH). I teraz, cała sztuczka polega na tym, ile tych grup -OH ma dany alkohol.
Alkohol monohydroksylowy, jak sama nazwa wskazuje (mono- oznacza jeden), to taki alkohol, który ma tylko jedną grupę hydroksylową (-OH) w swojej cząsteczce. Prosty przykład? Etanol, czyli alkohol, który znajduje się w piwie, winie i wódce. Wzór etanolu to CH3CH2OH. Widzisz, tylko jedna grupa -OH! Inne przykłady to metanol (CH3OH) i propanol (CH3CH2CH2OH).
Z kolei alkohol polihydroksylowy (poli- oznacza wiele), to taki alkohol, który ma więcej niż jedną grupę hydroksylową (-OH) w swojej cząsteczce. Bardzo popularny przykład to glikol etylenowy (CH2OHCH2OH), który często używany jest jako płyn do chłodnic samochodowych. Ma dwie grupy -OH. Inny przykład to glicerol (CH2OHCHOHCH2OH), który ma aż trzy grupy -OH. Glicerol jest składnikiem wielu kosmetyków.
Jak więc je odróżnić?
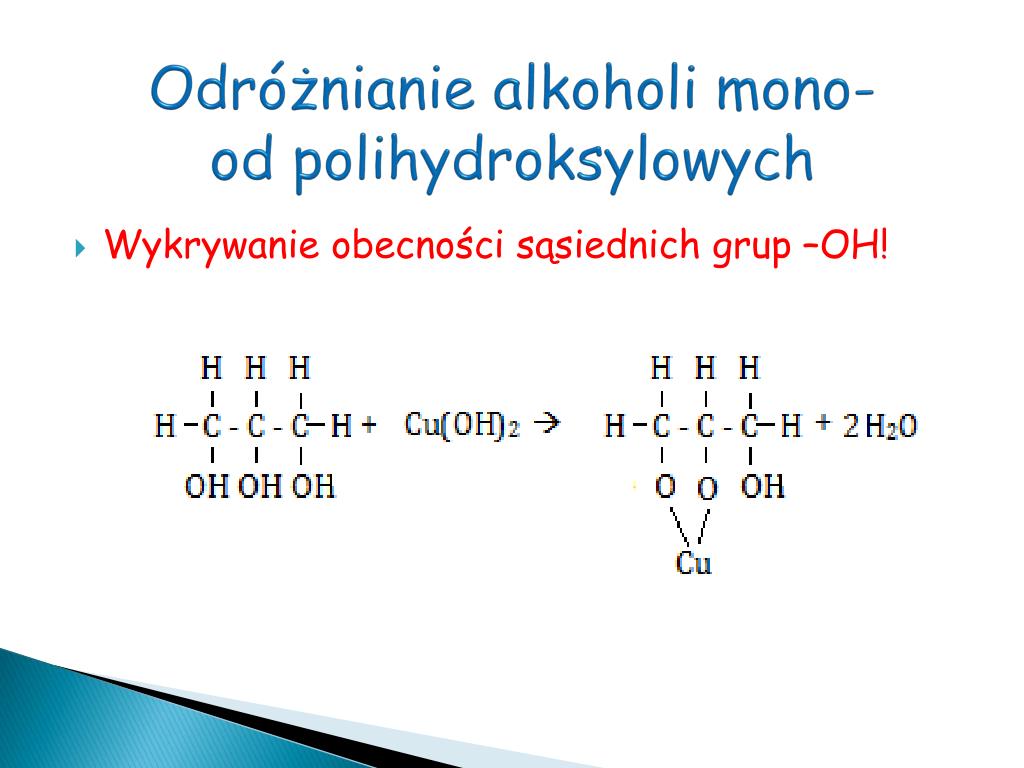
Najprościej jest, oczywiście, spojrzeć na wzór strukturalny. Jeśli widzisz tylko jedną grupę -OH, to masz do czynienia z alkoholem monohydroksylowym. Jeśli widzisz więcej grup -OH, to masz do czynienia z alkoholem polihydroksylowym.
Ale co, jeśli nie masz pod ręką wzoru? Wtedy trzeba sięgnąć po pewne metody oparte na właściwościach chemicznych i fizycznych tych alkoholi.
Właściwości fizyczne
Alkohole polihydroksylowe, ze względu na większą liczbę grup -OH, tworzą więcej wiązań wodorowych. Co to oznacza?
- Wyższa temperatura wrzenia: Wiązania wodorowe są "silniejsze" i trudniej je rozerwać, więc trzeba dostarczyć więcej energii (ciepła), żeby alkohol polihydroksylowy przeszedł w stan gazowy. Na przykład, etanol (monohydroksylowy) wrze w temperaturze około 78 stopni Celsjusza, a glikol etylenowy (dihydroksylowy) wrze w temperaturze około 197 stopni Celsjusza! Glicerol, z trzema grupami -OH, wrze jeszcze wyżej.
- Większa lepkość: Wiązania wodorowe "sklejają" cząsteczki alkoholu polihydroksylowego ze sobą, przez co trudniej im się przemieszczać. Stąd, alkohole polihydroksylowe są zazwyczaj bardziej lepkie niż alkohole monohydroksylowe. Weź na przykład miód, który jest lepki, bo zawiera cukry, które są polihydroksylowymi alkoholami.
- Lepsza rozpuszczalność w wodzie: Grupy -OH bardzo dobrze "dogadują się" z wodą (woda też tworzy wiązania wodorowe!). Im więcej grup -OH, tym lepiej dany alkohol rozpuszcza się w wodzie. Alkohole monohydroksylowe, zwłaszcza te o długich łańcuchach węglowych, mogą rozpuszczać się w wodzie gorzej.
Reakcje chemiczne
Chociaż grupy -OH we wszystkich alkoholach reagują podobnie, istnieją pewne reakcje, które mogą pomóc w odróżnieniu alkoholi monohydroksylowych od polihydroksylowych.
-
Reakcja z metalami aktywnymi: Zarówno alkohole monohydroksylowe, jak i polihydroksylowe reagują z metalami aktywnymi, takimi jak sód (Na) czy potas (K), wydzielając wodór (H2). Im więcej grup -OH w cząsteczce alkoholu, tym więcej wodoru zostanie wydzielone. Można to zaobserwować w postaci pęcherzyków gazu. Jednak, ilość wydzielonego wodoru jest proporcjonalna do ilości alkoholu, więc samo zaobserwowanie pęcherzyków nic nie mówi o rodzaju alkoholu bez dokładnych pomiarów.
2H2
-
Estryfikacja: Alkohole reagują z kwasami karboksylowymi, tworząc estry i wodę. Jest to reakcja estryfikacji. Alkohole polihydroksylowe mogą tworzyć bardziej złożone estry, ponieważ każda grupa -OH może reagować z inną cząsteczką kwasu. Przykładowo, glicerol może reagować z trzema cząsteczkami kwasu, tworząc triestry.
Podsumowując:
- Wzór: Najprostsza metoda - sprawdź wzór strukturalny. Jedna grupa -OH to alkohol monohydroksylowy, więcej niż jedna to alkohol polihydroksylowy.
- Właściwości fizyczne: Alkohole polihydroksylowe mają zazwyczaj wyższe temperatury wrzenia, większą lepkość i lepszą rozpuszczalność w wodzie niż alkohole monohydroksylowe o podobnej masie cząsteczkowej.
- Reakcje chemiczne: Obserwuj ilość wydzielonego wodoru w reakcji z metalami aktywnymi lub możliwość tworzenia bardziej złożonych estrów.
Praktyczne wskazówki:
Wyobraź sobie, że masz dwie bezbarwne ciecze. Jedna to etanol (alkohol monohydroksylowy), a druga to glicerol (alkohol polihydroksylowy).
- Wygląd i konsystencja: Glicerol będzie bardziej lepki niż etanol. Jeśli przechylisz butelkę z glicerolem, zobaczysz, że spływa wolniej niż etanol.
- Rozpuszczalność w wodzie: Obydwie ciecze dobrze rozpuszczają się w wodzie, ale glicerol (polihydroksylowy) będzie mieszał się z wodą łatwiej i szybciej.
- Temperatura wrzenia (teoretycznie): Gdybyś miał możliwość zagotowania tych cieczy (co nie jest zalecane bez odpowiedniego sprzętu i wiedzy!), zauważyłbyś, że etanol wrze w niższej temperaturze niż glicerol.
Mam nadzieję, że teraz rozumiesz, jak odróżnić alkohole monohydroksylowe od polihydroksylowych! To kwestia spojrzenia na ich strukturę, właściwości fizyczne i chemiczne. Pamiętaj, że chemia może być fascynująca!