Jak Obliczyć Rozmieszczenie Elektronów Na Powłokach

Oto artykuł napisany zgodnie z podanymi wytycznymi:
Rozmieszczenie elektronów na powłokach to fundament zrozumienia zachowania atomów i tworzenia wiązań chemicznych. Uczenie tego zagadnienia może być wyzwaniem, ale z odpowiednimi strategiami i podejściem można sprawić, że stanie się ono fascynującą podróżą w głąb mikroświata. Niniejszy artykuł ma na celu przedstawienie praktycznych wskazówek dla nauczycieli, jak efektywnie przekazywać wiedzę na temat konfiguracji elektronowej.
Podstawy Teoretyczne – Krótkie Przypomnienie
Zacznijmy od fundamentów. Atom składa się z jądra zawierającego protony i neutrony, wokół którego krążą elektrony. Elektrony nie poruszają się w sposób przypadkowy; zajmują określone poziomy energetyczne, nazywane powłokami elektronowymi. Powłoki te oznaczamy liczbami naturalnymi (n = 1, 2, 3, ...) lub literami (K, L, M, ...). Powłoka najbliższa jądra (n=1, powłoka K) ma najniższą energię, a każda kolejna powłoka ma energię wyższą.
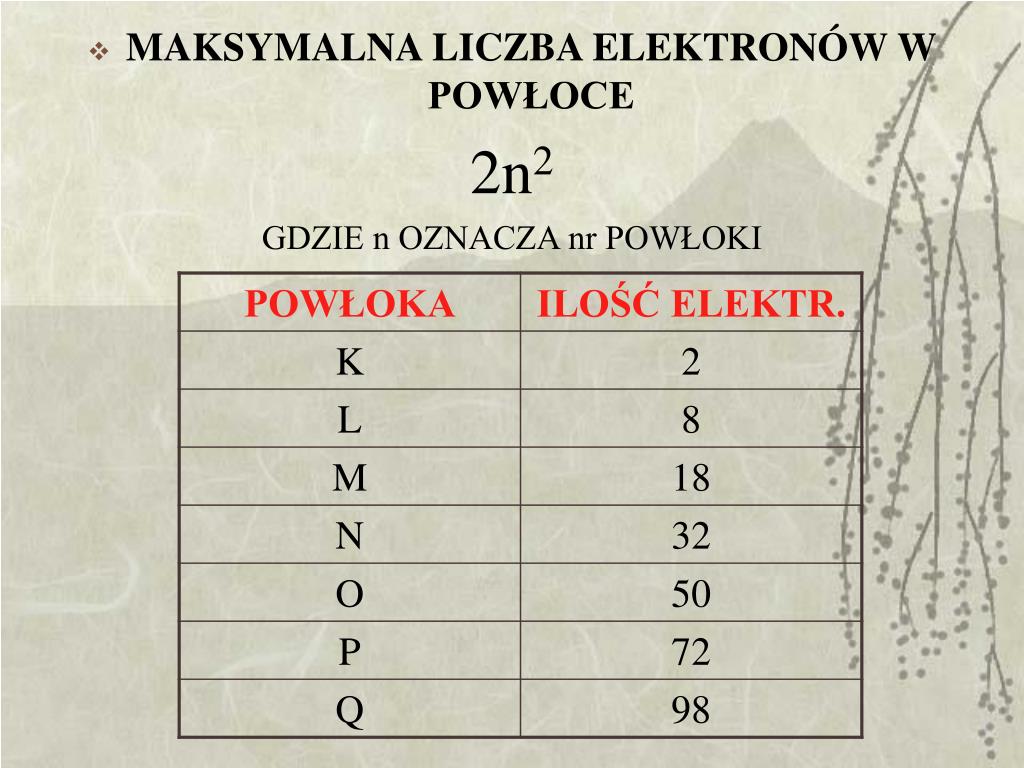
Maksymalna liczba elektronów, którą może pomieścić dana powłoka, określona jest wzorem 2n², gdzie n to numer powłoki. Zatem:
- Powłoka K (n=1): 2 * 1² = 2 elektrony
- Powłoka L (n=2): 2 * 2² = 8 elektronów
- Powłoka M (n=3): 2 * 3² = 18 elektronów
- Powłoka N (n=4): 2 * 4² = 32 elektrony
Ważne jest, aby podkreślić, że reguła 2n² jest ogólną zasadą, ale w przypadku pierwiastków o wyższej liczbie atomowej konfiguracja elektronowa staje się bardziej złożona i nie zawsze jest z nią zgodna. Dlatego na poziomie szkoły podstawowej i wczesnej szkoły średniej często upraszcza się model.
Jak Uczyć o Konfiguracji Elektronowej – Praktyczne Porady
-
Zaczynaj od modelu atomu: Przed wprowadzeniem pojęcia powłok elektronowych, upewnij się, że uczniowie rozumieją podstawową strukturę atomu: jądro z protonami i neutronami oraz elektrony krążące wokół. Można użyć prostych modeli atomów (np. wykonanych z piłeczek pingpongowych i koralików) lub animacji komputerowych.
-
Wprowadź pojęcie powłok stopniowo: Nie od razu zasypuj uczniów wzorami i skomplikowanymi zasadami. Zacznij od przedstawienia powłok jako „poziomów energetycznych”, na których znajdują się elektrony. Wykorzystaj analogię do schodów – elektrony mogą zajmować tylko określone „stopnie” (powłoki), a nie miejsca pomiędzy nimi.
-
Wykorzystaj schematy i diagramy: Wizualizacja jest kluczowa. Rysuj na tablicy schematy atomów z zaznaczonymi powłokami i elektronami. Można użyć kropek lub krzyżyków do reprezentowania elektronów. Dobrym pomysłem jest wykorzystanie diagramów energetycznych, które pokazują względną energię poszczególnych powłok.
-
Ćwiczenia praktyczne – konfiguracja dla pierwiastków: Po wprowadzeniu podstawowych zasad, przejdź do ćwiczeń praktycznych. Zacznij od prostych pierwiastków, takich jak wodór (H), hel (He), lit (Li), beryl (Be), bor (B), węgiel (C), azot (N), tlen (O), fluor (F), neon (Ne), sód (Na), magnez (Mg). Pokazuj krok po kroku, jak rozmieszczać elektrony na powłokach, bazując na liczbie atomowej (liczbie protonów, która jest równa liczbie elektronów w atomie obojętnym).
- Przykład: Sód (Na), liczba atomowa 11. Posiada 11 elektronów. Powłoka K (n=1) może pomieścić 2 elektrony. Powłoka L (n=2) może pomieścić 8 elektronów. Pozostaje 1 elektron, który umieszczamy na powłoce M (n=3). Konfiguracja elektronowa sodu: 2, 8, 1.
-
Wyjaśnij pojęcie elektronów walencyjnych: Podkreśl znaczenie elektronów znajdujących się na ostatniej powłoce (elektronów walencyjnych). To one decydują o właściwościach chemicznych pierwiastka i jego zdolności do tworzenia wiązań.
-
Zastosuj modele interaktywne: Dostępne są różne programy komputerowe i symulacje online, które pozwalają uczniom samodzielnie budować modele atomów i rozmieszczać elektrony na powłokach. To bardzo angażujący sposób na naukę.
-
Gry i zabawy edukacyjne: Wykorzystaj gry i zabawy, aby utrwalić wiedzę. Można zorganizować quizy, konkursy lub gry planszowe, w których zadaniem uczniów jest poprawne określenie konfiguracji elektronowej danego pierwiastka.
-
Odwołuj się do życia codziennego: Staraj się pokazywać, jak wiedza o konfiguracji elektronowej przekłada się na zrozumienie zjawisk zachodzących w życiu codziennym. Na przykład, wyjaśnij, jak właściwości metali (dobre przewodnictwo elektryczne i cieplne) wynikają z ich konfiguracji elektronowej i łatwości oddawania elektronów walencyjnych.
-
Zastosuj techniki mnemotechniczne: Pomagają zapamiętać kolejność zapełniania powłok i podpowłok. Na przykład, wymyśl hasło lub rymowankę związaną z tą kolejnością.
Typowe Błędy i Jak Ich Unikać
- Mylenie liczby atomowej z liczbą masową: Upewnij się, że uczniowie rozumieją różnicę między liczbą atomową (liczba protonów) a liczbą masową (liczba protonów i neutronów). Konfiguracja elektronowa zależy od liczby atomowej.
- Uważanie, że każda powłoka musi być w pełni zapełniona, zanim elektrony zaczną zajmować następną: Wyjaśnij, że powłoki zapełniane są zgodnie z zasadą minimalnej energii, a czasami bardziej stabilna jest konfiguracja, w której powłoka nie jest w pełni zapełniona, ale ma zapełnioną podpowłokę (np. d5 lub d10). To jednak zagadnienie na bardziej zaawansowanym poziomie.
- Błędne stosowanie wzoru 2n²: Pamiętaj, aby przypomnieć, że wzór 2n² określa maksymalną liczbę elektronów, jaką może pomieścić dana powłoka, a nie liczbę elektronów, która musi się na niej znajdować.
- Przeładowanie informacjami: Staraj się unikać zbyt wielu szczegółów na raz. Zacznij od podstaw, a następnie stopniowo wprowadzaj bardziej złożone koncepcje, takie jak podpowłoki i orbitale (jeśli to konieczne na danym poziomie nauczania).
Angażujące Metody Nauczania
-
Budowanie modeli atomów z materiałów recyklingowych: Zachęć uczniów do kreatywności i wykorzystania materiałów recyklingowych (np. pudełka, koraliki, styropianowe kulki) do zbudowania modeli atomów. To nie tylko uczy o strukturze atomu, ale także promuje świadomość ekologiczną.
-
"Konfiguracja elektronowa" – gra planszowa: Stwórz grę planszową, w której uczniowie poruszają się po planszy reprezentującej kolejne powłoki elektronowe. Odpowiedzi na pytania dotyczące konfiguracji elektronowej pozwalają im przesuwać się do przodu.
-
Debata "Elektrony walencyjne – klucz do wszystkiego": Zorganizuj debatę, w której uczniowie dyskutują na temat znaczenia elektronów walencyjnych dla właściwości chemicznych pierwiastków. Podziel uczniów na dwie grupy – jedna argumentuje za, a druga przeciwko tezie.
-
Projekt badawczy "Pierwiastki wokół nas": Poproś uczniów o przeprowadzenie projektu badawczego, w którym zbadają występowanie różnych pierwiastków w ich otoczeniu i powiążą to z ich konfiguracją elektronową i właściwościami.
-
Użycie analogii do systemu słonecznego: Wykorzystaj analogię do systemu słonecznego, gdzie jądro atomowe jest jak Słońce, a elektrony krążą wokół niego jak planety. Pamiętaj jednak, że ta analogia ma ograniczenia, ponieważ elektrony nie krążą po ściśle określonych orbitach.
Konkluzja
Nauczanie o rozmieszczeniu elektronów na powłokach to proces, który wymaga cierpliwości, kreatywności i dostosowania do poziomu uczniów. Kluczem do sukcesu jest stopniowe wprowadzanie pojęć, wykorzystywanie wizualizacji, ćwiczenia praktyczne i angażowanie uczniów w proces nauki. Poprzez unikanie typowych błędów i stosowanie angażujących metod nauczania, możemy sprawić, że uczniowie zrozumieją i zapamiętają zasady konfiguracji elektronowej, co z kolei otworzy im drzwi do dalszej eksploracji fascynującego świata chemii. Należy pamiętać, że uproszczenia są często konieczne na wczesnym etapie nauki, ale ważne jest, aby uczniowie byli świadomi, że pełny obraz jest bardziej złożony.