Jak Obliczyć Kationy I Aniony

W chemii, zrozumienie koncepcji kationów i anionów jest fundamentalne. Są to jony – atomy lub grupy atomów, które zyskały lub straciły elektrony, uzyskując ładunek elektryczny. Kationy mają ładunek dodatni, a aniony mają ładunek ujemny. Wiedza o tym, jak je obliczyć, jest kluczowa do przewidywania reakcji chemicznych, zrozumienia właściwości związków jonowych i interpretowania danych laboratoryjnych. Niniejszy artykuł omawia szczegółowo metody identyfikacji i obliczania ilości kationów i anionów.
Różnica między kationami a anionami
Podstawowa różnica między kationami a anionami leży w ich ładunku elektrycznym.
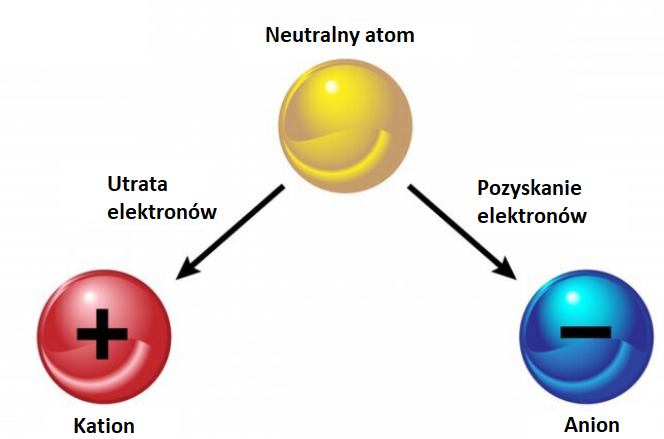
- Kationy: Powstają, gdy atom traci jeden lub więcej elektronów. Ponieważ elektrony mają ładunek ujemny, utrata elektronów powoduje, że atom uzyskuje nadmiar protonów, co daje mu ładunek dodatni. Przykłady: Na+ (jon sodu), Ca2+ (jon wapnia), Al3+ (jon glinu).
- Aniony: Powstają, gdy atom zyskuje jeden lub więcej elektronów. Zyskanie elektronów prowadzi do nadmiaru elektronów w porównaniu z protonami, co daje atomowi ładunek ujemny. Przykłady: Cl- (jon chlorkowy), O2- (jon tlenkowy), SO42- (jon siarczanowy).
Elektrony walencyjne i tworzenie jonów
Tworzenie kationów i anionów jest silnie związane z elektronami walencyjnymi – elektronami znajdującymi się na najbardziej zewnętrznej powłoce elektronowej atomu. Atomy dążą do osiągnięcia stabilnej konfiguracji elektronowej, zazwyczaj takiej, w której ich najbardziej zewnętrzna powłoka jest całkowicie zapełniona (reguła oktetu lub duetu). Dlatego atomy chętnie tracą lub zyskują elektrony, aby osiągnąć tę stabilność.
Na przykład, sód (Na) ma jeden elektron walencyjny. Łatwiej jest mu stracić ten jeden elektron i stać się Na+, niż zyskać siedem elektronów, aby zapełnić swoją zewnętrzną powłokę. Z kolei chlor (Cl) ma siedem elektronów walencyjnych. Łatwiej jest mu zyskać jeden elektron i stać się Cl- niż stracić siedem.
Jak obliczyć liczbę kationów i anionów?
Obliczanie liczby kationów i anionów w roztworze lub związku chemicznym wymaga różnych podejść, w zależności od dostępnych informacji. Najczęściej stosowane metody opisano poniżej:
Obliczenia stechiometryczne w związkach jonowych
Związki jonowe składają się z kationów i anionów połączonych wiązaniami jonowymi. Wzór chemiczny związku jonowego informuje o stosunku ilościowym między kationami i anionami. Na przykład, w chlorku sodu (NaCl) stosunek Na+ do Cl- wynosi 1:1. W chlorku wapnia (CaCl2) stosunek Ca2+ do Cl- wynosi 1:2. Oznacza to, że na jeden jon wapnia (Ca2+) przypadają dwa jony chlorkowe (Cl-).
Aby obliczyć liczbę kationów i anionów w danej masie związku jonowego, można użyć następujących kroków:
- Oblicz masę molową związku.
- Oblicz liczbę moli związku w danej masie (masa / masa molowa).
- Użyj współczynników stechiometrycznych z wzoru chemicznego, aby określić liczbę moli każdego jonu.
- Pomnóż liczbę moli każdego jonu przez liczbę Avogadro (6.022 x 1023), aby uzyskać liczbę jonów.
Przykład: Oblicz liczbę jonów Na+ i Cl- w 58.44 g NaCl.
- Masa molowa NaCl = 22.99 g/mol (Na) + 35.45 g/mol (Cl) = 58.44 g/mol
- Liczba moli NaCl = 58.44 g / 58.44 g/mol = 1 mol
- Z wzoru NaCl wynika, że 1 mol NaCl zawiera 1 mol Na+ i 1 mol Cl-.
- Liczba jonów Na+ = 1 mol * 6.022 x 1023 jonów/mol = 6.022 x 1023 jonów.
- Liczba jonów Cl- = 1 mol * 6.022 x 1023 jonów/mol = 6.022 x 1023 jonów.
Określanie stężeń jonów w roztworach
W roztworach jonowych, stężenie kationów i anionów jest wyrażane w jednostkach mol/L (molarność, M) lub mg/L (ppm – części na milion). Do obliczenia stężenia jonów można użyć następujących metod:
- Rozpuszczalność związków jonowych: Informacje o rozpuszczalności związków jonowych pozwalają na określenie maksymalnego stężenia jonów w roztworze. Na przykład, znając iloczyn rozpuszczalności (Ksp) trudno rozpuszczalnego związku, można obliczyć stężenie jonów w roztworze nasyconym.
- Analiza chemiczna: Techniki takie jak miareczkowanie, spektrometria absorpcji atomowej (AAS), chromatografia jonowa (IC) i potencjometria są wykorzystywane do pomiaru stężenia poszczególnych jonów w roztworach.
- Przewodnictwo elektrolityczne: Przewodnictwo elektryczne roztworu jest proporcjonalne do stężenia jonów. Pomiar przewodnictwa pozwala na oszacowanie stężenia jonów, chociaż metoda ta nie rozróżnia poszczególnych rodzajów jonów.
Przykład: Roztwór zawiera 0.1 M CaCl2. Oblicz stężenie Ca2+ i Cl- w roztworze.
Z wzoru CaCl2 wynika, że 1 mol CaCl2 dysocjuje na 1 mol Ca2+ i 2 mole Cl-. Dlatego:
- [Ca2+] = 0.1 M
- [Cl-] = 2 * 0.1 M = 0.2 M
Bilans ładunku elektrycznego
Zasada bilansu ładunku elektrycznego mówi, że w każdym roztworze elektrolitycznym suma ładunków dodatnich (kationów) musi być równa sumie ładunków ujemnych (anionów). Oznacza to, że roztwór jako całość jest elektrycznie obojętny. Można to zapisać następująco:
∑ (Stężenie kationu i * Ładunek i) = ∑ (Stężenie anionu j * |Ładunek j|)
Ta zasada jest bardzo przydatna do sprawdzania poprawności wyników analiz chemicznych i do obliczania nieznanych stężeń jonów, gdy znane są stężenia innych jonów.
Przykład: Roztwór zawiera Na+ (0.05 M) i Cl- (0.03 M). Oblicz stężenie SO42-.
Zasada bilansu ładunku: [Na+] * (+1) = [Cl-] * (-1) + [SO42-] * (-2)
0.05 = 0.03 + 2 * [SO42-]
[SO42-] = (0.05 - 0.03) / 2 = 0.01 M
Realne zastosowania
Zrozumienie i obliczanie kationów i anionów ma szerokie zastosowanie w różnych dziedzinach:
- Chemia analityczna: Oznaczanie składu chemicznego próbek środowiskowych (woda, gleba), żywności, leków.
- Chemia środowiska: Monitorowanie jakości wody, ocena zanieczyszczeń, badanie procesów biogeochemicznych. Na przykład, pomiar stężenia jonów azotanowych (NO3-) w wodach gruntowych w celu oceny zanieczyszczenia nawozami.
- Medycyna: Analiza elektrolitów w krwi (Na+, K+, Cl-) w celu diagnozowania i monitorowania chorób.
- Rolnictwo: Określanie zawartości składników odżywczych w glebie (K+, Ca2+, Mg2+) w celu optymalizacji nawożenia.
- Przemysł: Kontrola procesów technologicznych, analiza składu surowców i produktów. Na przykład, monitorowanie stężenia jonów chlorkowych w procesach produkcyjnych w przemyśle chemicznym.
Dane: Badanie stężenia jonów w próbkach wody pitnej ujawniło następujące wartości (w mg/L):
- Na+: 20
- Ca2+: 50
- Mg2+: 15
- Cl-: 30
- SO42-: 40
- HCO3-: 100
Analiza tych danych pozwala na ocenę twardości wody, zasolenia oraz potencjalnych źródeł zanieczyszczeń.
Wnioski
Zrozumienie koncepcji kationów i anionów oraz umiejętność ich obliczania są niezbędne w wielu dziedzinach nauki i techniki. Poprzez zrozumienie jak atomy zyskują lub tracą elektrony, tworząc jony, możemy przewidywać i interpretować reakcje chemiczne, analizować skład roztworów i materiałów, oraz kontrolować procesy przemysłowe. Zachęcamy do dalszego zgłębiania tej tematyki i wykorzystania zdobytej wiedzy w praktyce. Pamiętaj, że solidne zrozumienie podstaw chemii jest kluczem do rozwiązywania wielu problemów w otaczającym nas świecie.