Do Kalorymetru Zawierającego Mieszaninę Wody Z Lodem

Zanurzmy się w fascynujący świat kalorymetru, a konkretnie tego, który wykorzystuje mieszaninę wody z lodem. Taki kalorymetr oferuje unikalne możliwości i pewne wyzwania, które sprawiają, że jego zrozumienie jest kluczowe dla każdego, kto zajmuje się termochemią i pomiarami ciepła.
Budowa i Zasada Działania
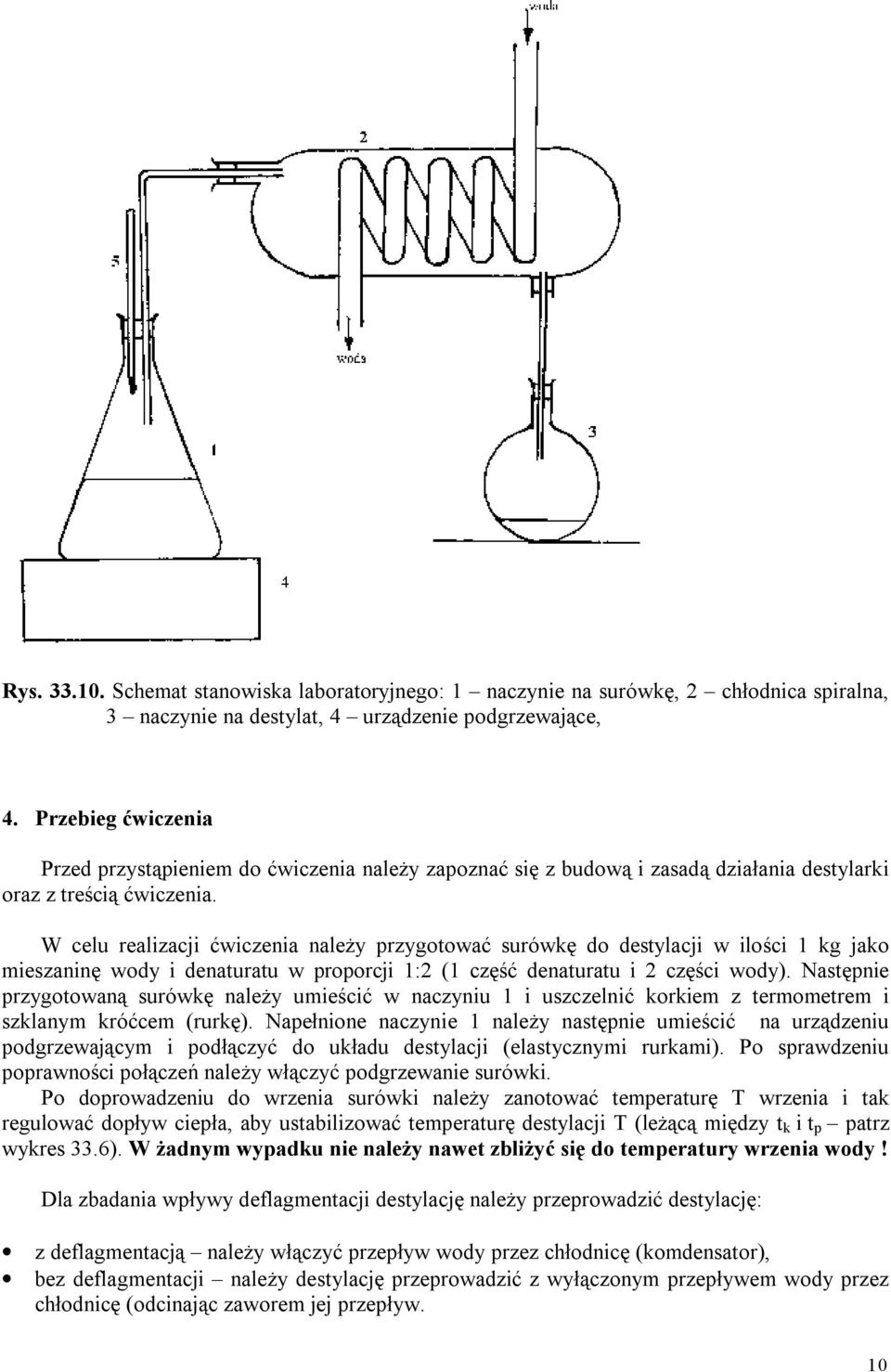
Wyobraź sobie naczynie termicznie izolowane od otoczenia. To serce naszego kalorymetru. Wewnątrz tego naczynia umieszczamy mieszaninę wody i lodu, utrzymywaną w stanie równowagi termicznej. Istotne jest, aby lód i woda pozostawały w kontakcie, a temperatura mieszaniny była bliska 0°C.
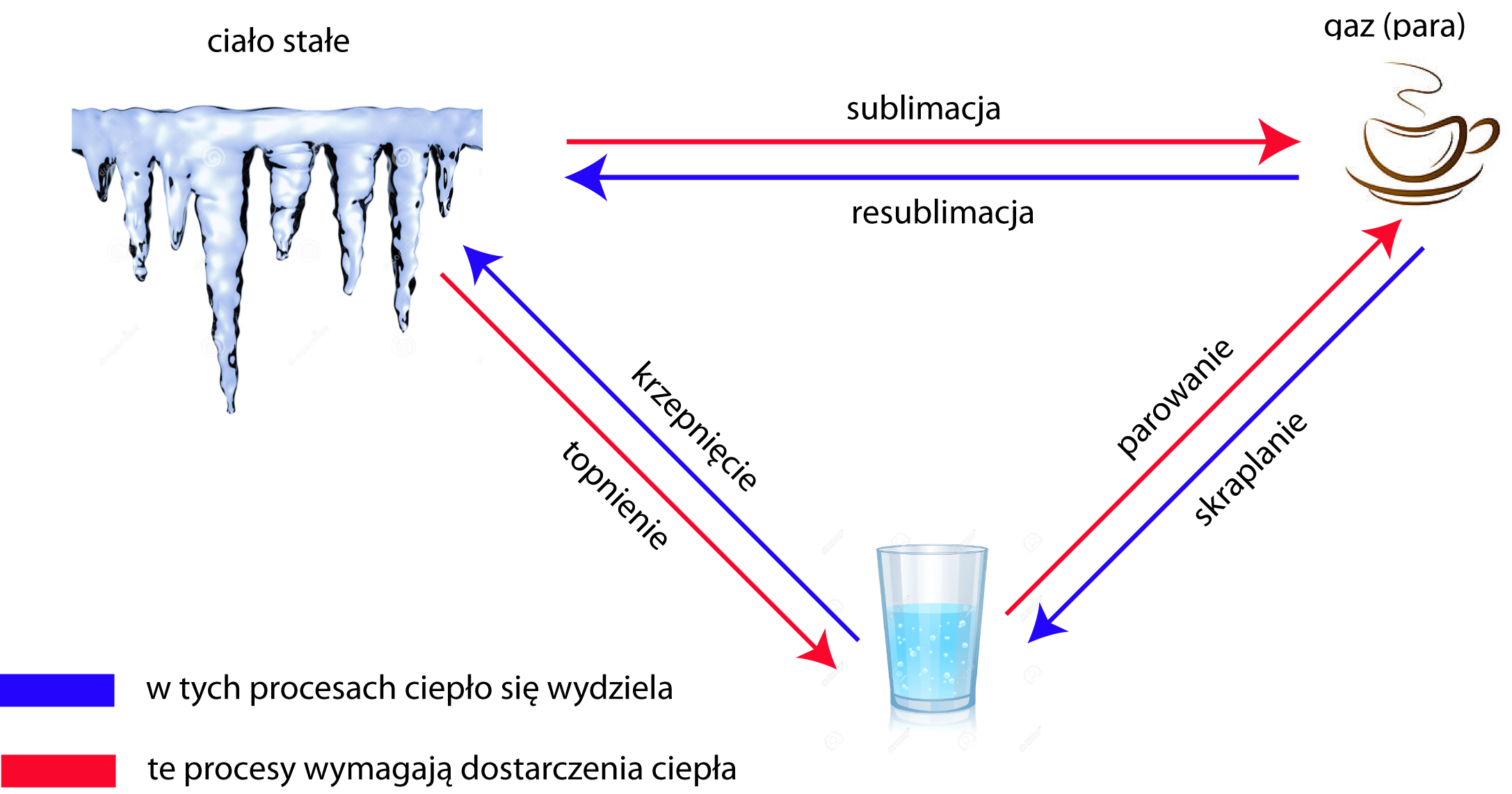
Kiedy do kalorymetru wprowadzamy próbkę, która oddaje ciepło (reakcja egzotermiczna lub po prostu ciepły obiekt), ciepło to jest absorbowane przez mieszaninę wody z lodem. Co się dzieje? Część lodu zaczyna się topić. Ilość stopionego lodu jest wprost proporcjonalna do ilości ciepła oddanego przez próbkę.
Kluczowym elementem jest precyzyjne określenie masy stopionego lodu. W jaki sposób to robimy? Mierzymy zmianę objętości mieszaniny wody z lodem. Wiemy, że woda ma większą gęstość niż lód. Zatem, stopienie lodu powoduje zmniejszenie objętości mieszaniny. Ta zmiana objętości, po odpowiednich przeliczeniach, pozwala nam wyznaczyć ilość ciepła uwolnionego w kalorymetrze.
Aby to zrealizować praktycznie, często stosuje się rurkę kapilarną połączoną z kalorymetrem. Zmiana objętości mieszaniny wody z lodem powoduje przesunięcie słupa cieczy w rurce kapilarnej. Odczytując to przesunięcie, możemy obliczyć zmianę objętości i, co za tym idzie, ilość stopionego lodu.
Zalety i Wady Kalorymetru Wodno-Lodowego
Kalorymetr wodno-lodowy ma pewne istotne zalety. Przede wszystkim, utrzymuje stałą temperaturę (0°C) podczas całego procesu pomiaru. To upraszcza obliczenia i minimalizuje błędy związane ze zmianą ciepła właściwego substancji. Ponadto, jest szczególnie przydatny do pomiaru ciepła reakcji zachodzących w pobliżu 0°C.
Jednakże, istnieją również wady. Przygotowanie kalorymetru do pracy jest czasochłonne i wymaga dużej precyzji. Musimy upewnić się, że mieszanina wody z lodem jest w stanie równowagi termicznej, a cały układ jest odpowiednio zaizolowany. Dodatkowo, pomiar zmiany objętości może być trudny i obarczony pewnymi błędami. Czynniki takie jak napięcie powierzchniowe cieczy w rurce kapilarnej czy niedokładność odczytu przesunięcia słupa cieczy mogą wpłynąć na wynik.
Dokładność pomiaru zależy również od czystości użytej wody i lodu. Zanieczyszczenia mogą wpływać na temperaturę topnienia lodu i na jego gęstość, co z kolei prowadzi do błędów w obliczeniach.
Kalorymetr wodno-lodowy jest również wrażliwy na wpływy zewnętrzne. Niewielkie zmiany temperatury otoczenia mogą powodować topnienie lodu lub zamarzanie wody, co zakłóca pomiar. Dlatego, konieczne jest stosowanie odpowiedniej izolacji termicznej i utrzymywanie stałej temperatury w pomieszczeniu, w którym przeprowadzany jest pomiar.
Obliczenia i Interpretacja Wyników
Po przeprowadzeniu pomiaru i określeniu masy stopionego lodu, możemy obliczyć ilość ciepła oddanego przez próbkę. Wykorzystujemy do tego ciepło topnienia lodu (L). Wzór jest prosty:
Q = m * L
gdzie:
- Q – ilość ciepła (w dżulach)
- m – masa stopionego lodu (w kilogramach)
- L – ciepło topnienia lodu (ok. 333.55 kJ/kg)
Otrzymana wartość Q odpowiada ciepłu, które zostało uwolnione lub zaabsorbowane podczas badanego procesu. Interpretacja wyniku zależy od rodzaju przeprowadzanego eksperymentu. Jeśli badamy ciepło reakcji chemicznej, Q odpowiada zmianie entalpii reakcji. Jeśli badamy ciepło oddane przez ciepły obiekt, Q odpowiada ilości ciepła, jaką obiekt stracił, obniżając swoją temperaturę.
Precyzja obliczeń jest kluczowa. Należy uwzględnić wszystkie możliwe źródła błędów, takie jak niedokładność pomiaru masy stopionego lodu, błędy związane z izolacją termiczną kalorymetru i ewentualne straty ciepła do otoczenia.
Praktyczne Aspekty Użytkowania Kalorymetru Wodno-Lodowego
Przygotowanie kalorymetru wodno-lodowego do pracy to proces wymagający cierpliwości i dokładności. Najpierw musimy przygotować czystą wodę destylowaną i lód, również wykonany z wody destylowanej. Istotne jest, aby lód był w postaci drobnych kawałków, co zapewni lepszy kontakt z wodą i szybsze osiągnięcie równowagi termicznej.
Następnie, mieszamy wodę z lodem w naczyniu kalorymetru, dbając o to, aby lód nie pływał po powierzchni wody, ale był równomiernie rozłożony w całej objętości. Po umieszczeniu mieszaniny w kalorymetrze, musimy odczekać pewien czas, aż układ osiągnie stan równowagi termicznej. Można to monitorować, obserwując wskazania termometru umieszczonego w kalorymetrze. Temperatura powinna ustabilizować się w pobliżu 0°C.
Przed wprowadzeniem próbki do kalorymetru, należy dokładnie zmierzyć jej masę i temperaturę. Jeśli próbka ma temperaturę inną niż 0°C, musimy uwzględnić ciepło, które odda lub pobierze, aby osiągnąć temperaturę równowagi.
Podczas wprowadzania próbki do kalorymetru, należy minimalizować straty ciepła do otoczenia. Można to zrobić, stosując odpowiednie narzędzia i działając szybko i sprawnie.
Po wprowadzeniu próbki, obserwujemy zmianę objętości mieszaniny wody z lodem. Odczytujemy przesunięcie słupa cieczy w rurce kapilarnej i obliczamy masę stopionego lodu. Na podstawie tej wartości, obliczamy ilość ciepła oddanego lub zaabsorbowanego przez próbkę.
Po zakończeniu pomiaru, kalorymetr należy dokładnie oczyścić i przygotować do kolejnego użycia. Należy usunąć stopiony lód i wodę, umyć naczynie i rurkę kapilarną, a następnie wysuszyć je.
Kalorymetr wodno-lodowy, choć nieco archaiczną, pozostaje cennym narzędziem w badaniach termochemicznych. Jego prosta zasada działania i stała temperatura pracy oferują unikalne możliwości pomiarowe, szczególnie w zakresie niskich temperatur. Opanowanie technik pracy z tym kalorymetrem stanowi solidną podstawę dla zrozumienia bardziej zaawansowanych metod kalorymetrycznych. Pomimo pewnych trudności związanych z przygotowaniem i obsługą, kalorymetr wodno-lodowy nadal znajduje zastosowanie w laboratoriach naukowych i dydaktycznych na całym świecie. Klucz do sukcesu leży w precyzji, cierpliwości i dokładnym zrozumieniu zasad termodynamiki.