Dlaczego Jedne Substancje Rozpuszczają Się W Wodzie A Inne Nie

Dzień dobry wszystkim! Widzę, że dzisiaj mamy bardzo ciekawe pytanie. Zastanawiacie się, dlaczego niektóre rzeczy bez problemu rozpuszczają się w wodzie, a inne za nic nie chcą? To tak, jakby woda miała swoich ulubieńców i tych, których woli unikać. Spróbuję wam to wytłumaczyć tak, żebyście zrozumieli to bez trudu.
Wyobraźcie sobie wodę jako wielką paczkę magnesów. Każdy magnes (czyli każda cząsteczka wody) ma dwa końce: jeden delikatnie naładowany dodatnio, a drugi delikatnie naładowany ujemnie. To właśnie sprawia, że woda jest taka wyjątkowa. Mówimy, że woda jest polarna. Teraz pomyślcie o innych substancjach, które próbujecie w wodzie rozpuścić. One też mogą być jak magnesy, albo zupełnie do nich niepodobne.
Żeby coś się rozpuściło w wodzie, musi "lubić" się z tymi wodnymi magnesami. Mówiąc prościej, musi mieć coś, co sprawi, że woda będzie chciała go "przyciągnąć" i rozdzielić na mniejsze części, aż zniknie w niej.
Co więc decyduje o tym, czy dana substancja "lubi" się z wodą? Głównie to, czy sama jest polarna, czy nie.
Substancje polarne i jonowe – ulubieńcy wody
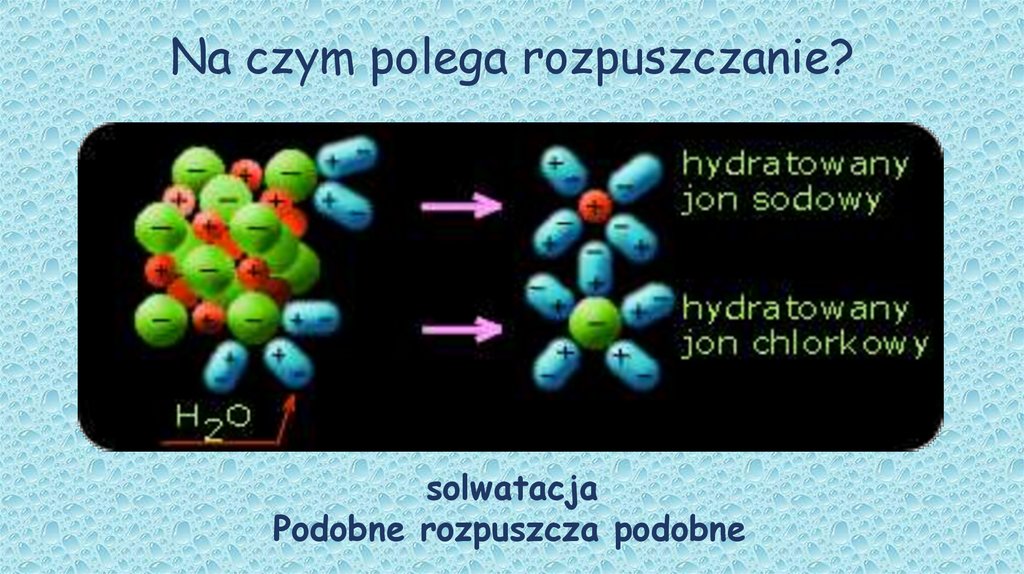
Substancje, które są podobne do wody, czyli również polarne, bardzo dobrze się w niej rozpuszczają. Dzieje się tak, ponieważ ich cząsteczki też mają naładowane końce, które przyciągają się do naładowanych końców cząsteczek wody. To tak, jakby magnes przyciągał magnes. Weźmy na przykład cukier (sacharozę). Cukier jest substancją polarną, dlatego cząsteczki wody z łatwością otaczają cząsteczki cukru i oddzielają je od siebie, aż cukier znika w wodzie. Podobnie dzieje się z solą kuchenną (chlorkiem sodu). Sól to związek jonowy. Związek jonowy to taki, który składa się z jonów – cząstek naładowanych dodatnio (kationów) i ujemnie (anionów). Kiedy sól wrzucamy do wody, woda rozdziela te jony (sód Na+ i chlor Cl-) i otacza je swoimi cząsteczkami. Dzieje się tak dlatego, że dodatnio naładowane jony sodu są przyciągane przez ujemne końce cząsteczek wody, a ujemnie naładowane jony chloru są przyciągane przez dodatnie końce cząsteczek wody. W efekcie sól rozpuszcza się w wodzie. Mówimy, że "podobne rozpuszcza się w podobnym". Polarne rozpuszcza polarne, a jonowe też dobrze radzą sobie w polarnych rozpuszczalnikach, takich jak woda.
Substancje niepolarne – odrzuceni przez wodę
Co się dzieje, gdy wrzucimy do wody coś, co nie jest polarne, czyli nie ma tych naładowanych końców? Wtedy woda nie ma "powodu", żeby to przyciągać i rozdzielać. Takie substancje, jak oleje, tłuszcze czy wosk, są niepolarne. Ich cząsteczki nie mają wyraźnie naładowanych końców, więc nie oddziałują z wodą tak silnie, jak substancje polarne czy jonowe. Woda "woli" trzymać się sama ze sobą, niż mieszać się z tymi "obcymi" cząsteczkami. Dlatego olej i woda się nie mieszają – olej unosi się na powierzchni, tworząc oddzielną warstwę.
Można to sobie wyobrazić tak: wyobraźcie sobie, że jesteście na przyjęciu, gdzie wszyscy się dobrze znają i trzymają się razem. Nagle przychodzi ktoś, kogo nikt nie zna i kto w ogóle nie pasuje do tej grupy. Nikt nie chce z nim rozmawiać, więc stoi samotnie z boku. Tak właśnie zachowuje się woda w stosunku do substancji niepolarnych.
Jak "oszukać" wodę?
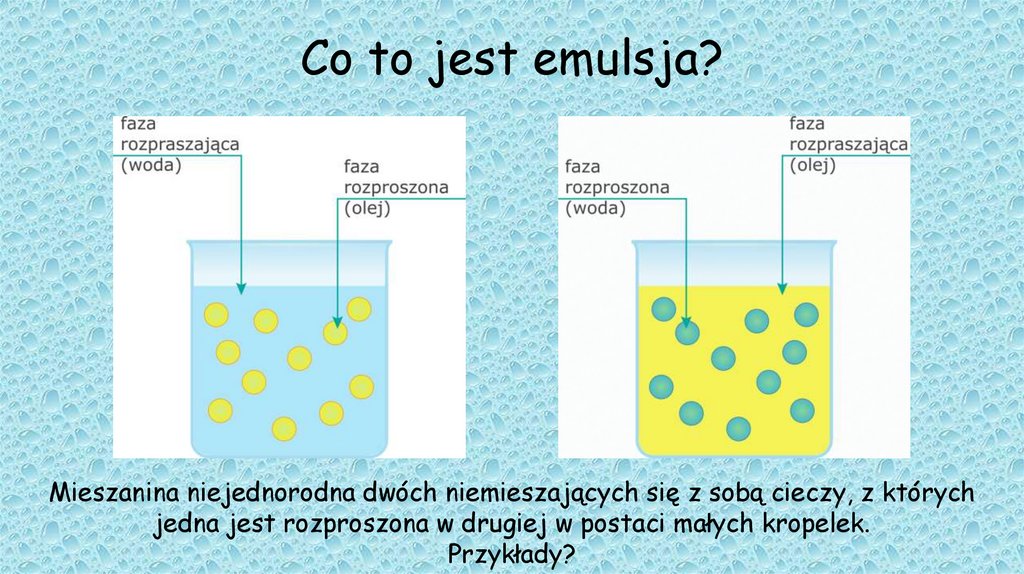
Czy da się zmusić wodę do rozpuszczenia czegoś, czego normalnie nie lubi? Czasami tak! Można użyć substancji, które mają część polarną i część niepolarną. Takie substancje nazywamy emulgatorami. Emulgatory mają jedną część, która "lubi" wodę (część polarna) i drugą część, która "lubi" tłuszcz (część niepolarna). Dzięki temu emulgator może połączyć wodę z tłuszczem, tworząc emulsję. Emulsja to mieszanina dwóch niemieszających się cieczy, w której jedna ciecz jest rozproszona w drugiej w postaci małych kropelek.
Przykładem emulgatora jest mydło. Mydło ma jedną część, która przyciąga wodę, i drugą część, która przyciąga tłuszcz i brud. Dlatego mydło pomaga usunąć tłuste plamy z ubrań – otacza cząsteczki tłuszczu i pozwala wodzie je spłukać. Innym przykładem jest żółtko jaja, które zawiera lecytynę – naturalny emulgator. Dlatego żółtko jaja jest używane do robienia majonezu, który jest emulsją oleju w wodzie.
Temperatura też ma znaczenie
Na rozpuszczalność ma również wpływ temperatura. Zazwyczaj, im wyższa temperatura, tym więcej substancji można rozpuścić w wodzie. Dzieje się tak dlatego, że podwyższona temperatura dostarcza więcej energii cząsteczkom wody, co pozwala im łatwiej pokonywać siły przyciągania między cząsteczkami rozpuszczanej substancji i rozdzielać je. Na przykład, więcej cukru rozpuści się w gorącej herbacie niż w zimnej. Jednak nie zawsze tak jest! W przypadku niektórych gazów, rozpuszczalność w wodzie maleje wraz ze wzrostem temperatury. Dlatego, gdy otwieramy butelkę ciepłej coli, wydobywa się z niej więcej bąbelków niż z zimnej.
Podsumowując, rozpuszczalność substancji w wodzie zależy głównie od tego, czy dana substancja jest polarna, czy nie. Substancje polarne i jonowe dobrze rozpuszczają się w wodzie, ponieważ oddziałują z polarnymi cząsteczkami wody. Substancje niepolarne nie rozpuszczają się w wodzie, ponieważ nie oddziałują z nią w wystarczającym stopniu. Można jednak "oszukać" wodę, używając emulgatorów, które łączą wodę z substancjami niepolarnymi. Temperatura również wpływa na rozpuszczalność, choć nie zawsze w ten sam sposób.
Mam nadzieję, że teraz lepiej rozumiecie, dlaczego niektóre substancje rozpuszczają się w wodzie, a inne nie. To tak naprawdę bardzo proste – wszystko zależy od tego, czy dana substancja "lubi" się z wodą, czy nie! A jeśli macie jeszcze jakieś pytania, to śmiało pytajcie!