Co To Jest Masa Cząsteczkowa

Czy kiedykolwiek zastanawiałeś się, jak chemicy mierzą rzeczy tak małe, jak cząsteczki? To może wydawać się niemożliwe, prawda? Wyobraź sobie, że próbujesz zważyć pojedyncze ziarnko piasku – to wyzwanie! Na szczęście, w chemii istnieje pojęcie masy cząsteczkowej, które umożliwia nam określenie masy tych mikroskopijnych struktur. Zrozumienie masy cząsteczkowej jest kluczowe nie tylko dla chemików, ale także dla wszystkich, którzy chcą zgłębić tajniki świata wokół nas, od lekarstw po materiały budowlane.
W tym artykule postaramy się wyjaśnić, czym dokładnie jest masa cząsteczkowa, jak ją obliczyć i dlaczego jest tak ważna. Postaramy się to zrobić w sposób przystępny i zrozumiały, unikając zbędnego żargonu chemicznego.
Czym jest Masa Cząsteczkowa?
Masa cząsteczkowa, nazywana również masą molową, to suma mas atomowych wszystkich atomów, które wchodzą w skład danej cząsteczki. Brzmi skomplikowanie? Spokojnie, rozłóżmy to na czynniki pierwsze. Pomyśl o cząsteczce jako o budynku zbudowanym z cegieł (atomów). Każda cegła ma swoją wagę. Masa cząsteczkowa to po prostu suma wag wszystkich cegieł użytych do budowy tego budynku.
Dokładniej, masę cząsteczkową wyraża się w jednostkach masy atomowej (u) lub gramach na mol (g/mol). Jednostka masy atomowej odnosi się do masy pojedynczej cząsteczki, natomiast gramy na mol odnoszą się do masy jednego mola cząsteczek (mol to około 6.022 x 1023 cząsteczek – liczba Avogadro). Użycie gramów na mol jest szczególnie przydatne w laboratorium, ponieważ umożliwia odważanie substancji w ilościach, które można zmierzyć na wadze.
Przykład: Cząsteczka wody (H2O) składa się z dwóch atomów wodoru (H) i jednego atomu tlenu (O). Masa atomowa wodoru wynosi około 1 u, a masa atomowa tlenu wynosi około 16 u. Zatem, masa cząsteczkowa wody wynosi (2 x 1 u) + (1 x 16 u) = 18 u. Oznacza to również, że 1 mol wody waży 18 gramów.
Jak Obliczyć Masę Cząsteczkową?
Obliczanie masy cząsteczkowej jest prostsze, niż mogłoby się wydawać. Oto kroki, które należy wykonać:
- Znajdź wzór chemiczny cząsteczki: To podstawa! Musisz wiedzieć, jakie atomy wchodzą w skład cząsteczki i ile ich jest. Na przykład, wzór glukozy to C6H12O6.
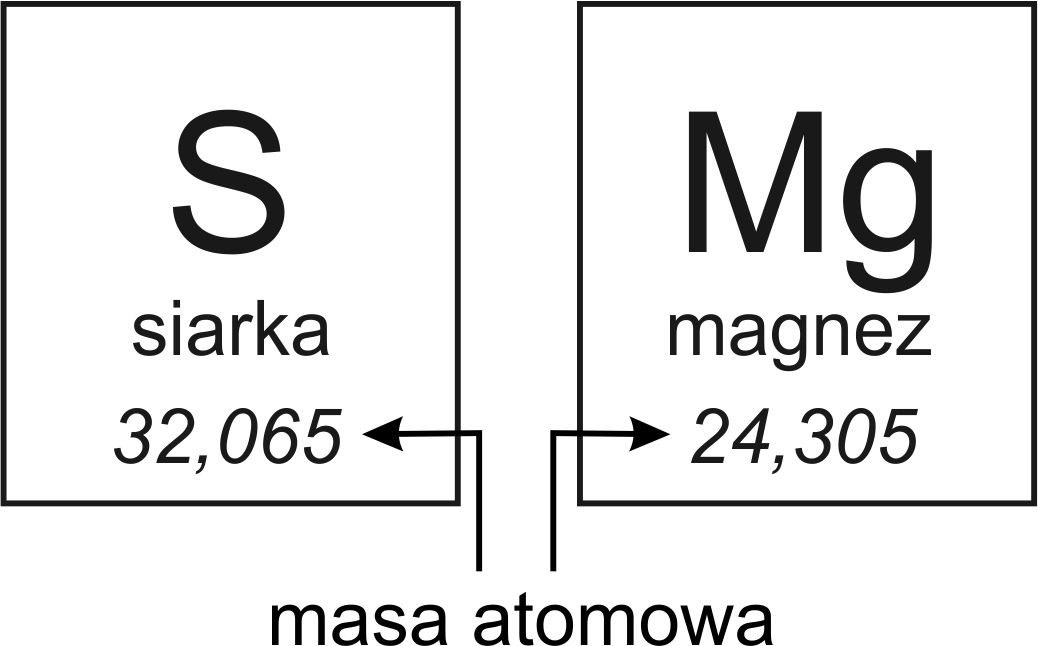
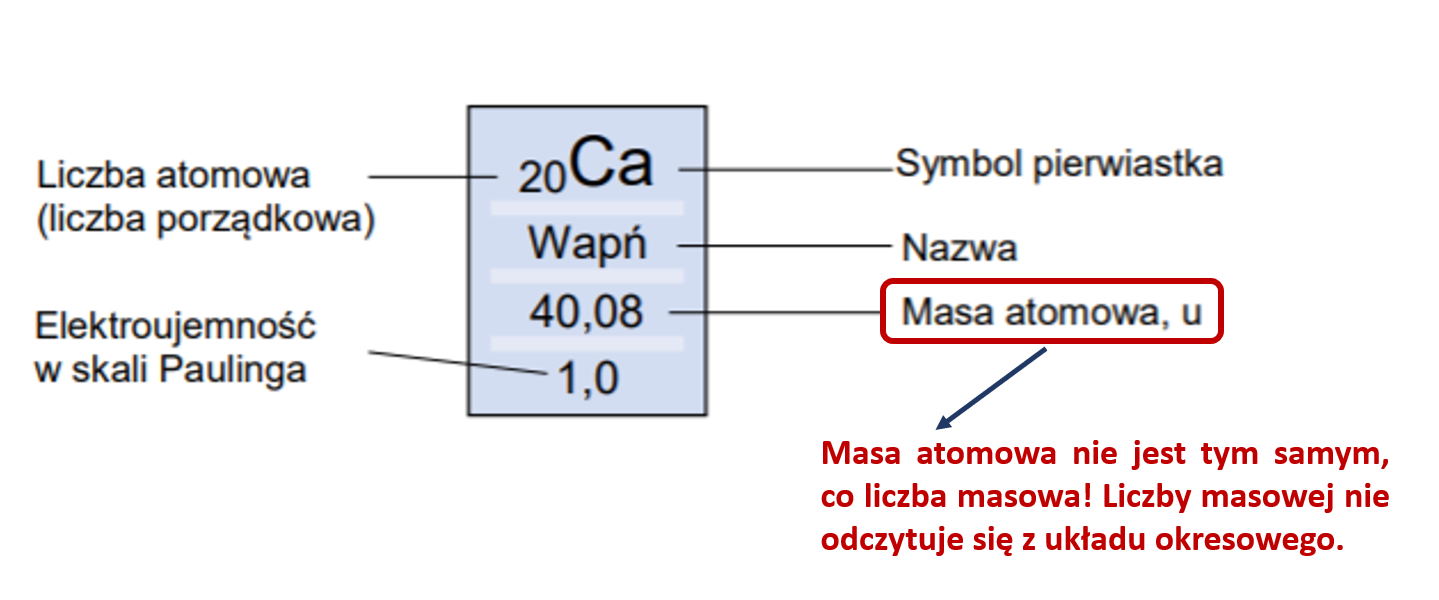
- Znajdź masy atomowe każdego pierwiastka: Możesz to zrobić, korzystając z układu okresowego pierwiastków. Większość układów okresowych podaje masy atomowe pod symbolem pierwiastka. Masa atomowa to średnia masa atomów danego pierwiastka, uwzględniająca naturalną zawartość izotopów.
- Pomnóż masę atomową każdego pierwiastka przez liczbę jego atomów w cząsteczce: Na przykład, w glukozie masz 6 atomów węgla, więc pomnóż masę atomową węgla (około 12 u) przez 6.
- Dodaj wszystkie wyniki: Suma tych iloczynów da ci masę cząsteczkową.
Przykład: Obliczmy masę cząsteczkową glukozy (C6H12O6):
- Węgiel (C): 6 atomów x 12 u/atom = 72 u
- Wodór (H): 12 atomów x 1 u/atom = 12 u
- Tlen (O): 6 atomów x 16 u/atom = 96 u
Masa cząsteczkowa glukozy: 72 u + 12 u + 96 u = 180 u. Oznacza to, że 1 mol glukozy waży 180 gramów.
Gdzie znaleźć masy atomowe?
Najłatwiej jest skorzystać z układu okresowego pierwiastków. Układy okresowe są dostępne w większości podręczników chemicznych, w laboratoriach, a także online (np. na stronach internetowych szkół, uniwersytetów, instytutów badawczych). W wielu aplikacjach chemicznych na smartfony również można znaleźć układ okresowy z masami atomowymi.
Dlaczego Masa Cząsteczkowa jest Ważna?
Masa cząsteczkowa to fundamentalna właściwość każdej substancji chemicznej i ma wiele zastosowań:
- Obliczenia stechiometryczne: Masa cząsteczkowa jest niezbędna do obliczeń stechiometrycznych, czyli obliczeń ilościowych w reakcjach chemicznych. Pozwala na określenie, ile substratów potrzeba, aby uzyskać określoną ilość produktu.
- Określanie składu procentowego: Dzięki masie cząsteczkowej możemy obliczyć skład procentowy każdego pierwiastka w danej substancji. To ważne np. przy analizie składu chemicznego próbek.
- Przygotowywanie roztworów: Masa cząsteczkowa jest kluczowa przy przygotowywaniu roztworów o określonym stężeniu molowym. Pozwala na odmierzenie odpowiedniej ilości substancji, aby uzyskać roztwór o żądanej koncentracji.
- Charakteryzacja związków chemicznych: Porównanie zmierzonej eksperymentalnie masy cząsteczkowej z wartością teoretyczną, obliczoną na podstawie wzoru chemicznego, pozwala na potwierdzenie tożsamości danej substancji.
- Badania naukowe: W badaniach naukowych, szczególnie w chemii i biologii, masa cząsteczkowa jest wykorzystywana do identyfikacji i charakteryzacji cząsteczek, np. białek, DNA, czy polimerów.
Przykład: W przemyśle farmaceutycznym masa cząsteczkowa leku jest kluczowa do określenia odpowiedniej dawki. Niedokładne obliczenia mogą prowadzić do podania zbyt małej dawki, która nie będzie skuteczna, lub zbyt dużej dawki, która może być toksyczna.
Masa Cząsteczkowa a Masa Atomowa Względna
Często mylone są pojęcia masy cząsteczkowej i masy atomowej względnej (Ar). Masa atomowa względna to bezwymiarowa wielkość, która wyraża masę atomu danego pierwiastka w stosunku do 1/12 masy atomu izotopu węgla 12C. Jest to wartość względna, dlatego nie ma jednostki. Masa atomowa względna jest wartością, którą znajdziemy w układzie okresowym pierwiastków.
Masa cząsteczkowa to suma mas atomowych wszystkich atomów wchodzących w skład cząsteczki i wyrażana jest w jednostkach masy atomowej (u) lub gramach na mol (g/mol). Zatem, masa cząsteczkowa jest wartością bezwzględną, odnoszącą się do konkretnej ilości substancji.
W praktyce, do obliczania masy cząsteczkowej wykorzystujemy masy atomowe (a dokładniej masy atomowe względne), ale pamiętajmy o różnicy w interpretacji tych pojęć.
Praktyczne Porady i Wskazówki
- Używaj dokładnych wartości mas atomowych: W zależności od wymagań precyzji obliczeń, możesz używać wartości mas atomowych z różną dokładnością. Im bardziej precyzyjne obliczenia, tym dokładniejsze powinny być używane masy atomowe.
- Zwracaj uwagę na wzór chemiczny: Upewnij się, że wzór chemiczny, którego używasz do obliczeń, jest poprawny. Błąd we wzorze chemicznym doprowadzi do błędnego wyniku.
- Sprawdzaj jednostki: Pamiętaj o używaniu odpowiednich jednostek (u lub g/mol). Nie pomyl jednostek masy atomowej z gramami na mol.
- Korzystaj z kalkulatorów online: Istnieje wiele kalkulatorów online, które automatycznie obliczają masę cząsteczkową na podstawie wzoru chemicznego. Są to przydatne narzędzia, szczególnie przy obliczaniu masy cząsteczkowej skomplikowanych związków.
- Ćwicz obliczenia: Najlepszym sposobem na opanowanie obliczania masy cząsteczkowej jest ćwiczenie na przykładach. Im więcej przykładów rozwiążesz, tym pewniej będziesz się czuł w wykonywaniu tych obliczeń.
Podsumowanie
Zrozumienie masy cząsteczkowej jest kluczowe dla każdego, kto interesuje się chemią lub pokrewnymi dziedzinami. Od obliczeń stechiometrycznych po przygotowywanie roztworów, masa cząsteczkowa odgrywa fundamentalną rolę. Mam nadzieję, że ten artykuł pomógł Ci zrozumieć, czym jest masa cząsteczkowa, jak ją obliczyć i dlaczego jest tak ważna. Pamiętaj, że praktyka czyni mistrza! Ćwicz obliczenia, korzystaj z dostępnych narzędzi i nie bój się zadawać pytań. Powodzenia!