Chemia Wodorotlenki Klasa 8
Witaj! Jeśli jesteś w ósmej klasie i właśnie zagłębiasz się w świat chemii, a konkretnie w wodorotlenki, to wiesz, że może to być trochę... zagmatwane. Wzory, nazewnictwo, właściwości... Wszystko to może wydawać się na początku trudne do ogarnięcia. Ale spokojnie, nie jesteś sam! Wielu uczniów ma podobne odczucia. Postaram się to wszystko wytłumaczyć w prosty i przystępny sposób.
Pamiętaj, że chemia, choć może wydawać się abstrakcyjna, ma ogromny wpływ na nasze codzienne życie. Od leków, które nas leczą, po materiały, z których zbudowane są nasze domy, chemia jest wszędzie! Zrozumienie podstaw, takich jak wodorotlenki, otwiera drzwi do lepszego poznania świata.
Czym właściwie są wodorotlenki?
Wyobraź sobie wodę (H₂O). Wodorotlenek, to w pewnym sensie pochodna wody. Jest to związek chemiczny składający się z metalu (lub grupy amonowej NH₄) oraz grupy wodorotlenowej (OH⁻). Ta grupa OH⁻ jest kluczowa, bo to właśnie ona nadaje wodorotlenkom ich charakterystyczne właściwości.
Formalnie, wodorotlenki to związki jonowe, w których anionem jest właśnie anion wodorotlenkowy OH⁻, a kationem jest jon metalu. We wzorze chemicznym najpierw piszemy symbol metalu, a potem grupę wodorotlenową. Na przykład: NaOH (wodorotlenek sodu).
Dlaczego "wodorotlenek"?
Nazwa "wodorotlenek" pochodzi od obecności atomu wodoru (H) i atomu tlenu (O) w grupie OH⁻. To połączenie jest właśnie wodorotlenkiem.
Nazewnictwo wodorotlenków
Nazewnictwo wodorotlenków jest stosunkowo proste. Zaczynamy od słowa "wodorotlenek", a następnie podajemy nazwę metalu. Na przykład:
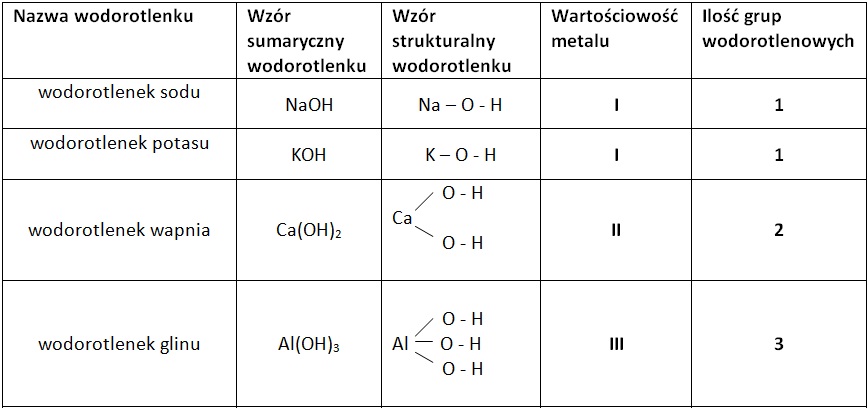
- NaOH - Wodorotlenek sodu
- KOH - Wodorotlenek potasu
- Ca(OH)₂ - Wodorotlenek wapnia
Jeśli metal w wodorotlenku ma więcej niż jedną wartościowość (czyli tworzy jony o różnym ładunku), musimy to zaznaczyć w nazwie, podając wartościowość metalu w nawiasie cyframi rzymskimi. Na przykład:
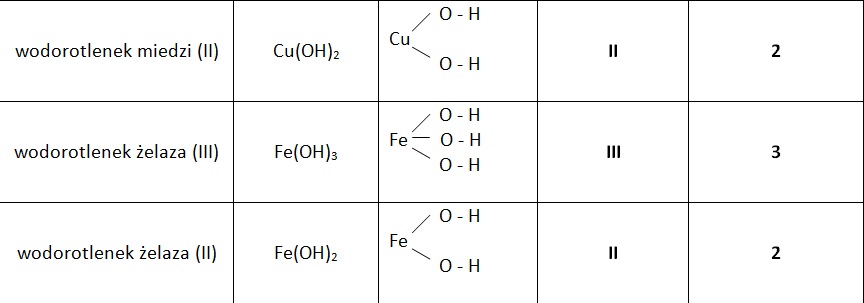
- Fe(OH)₂ - Wodorotlenek żelaza(II)
- Fe(OH)₃ - Wodorotlenek żelaza(III)
Wartościowość grupy wodorotlenowej (OH⁻) zawsze wynosi -1. Dlatego, aby napisać poprawny wzór sumaryczny wodorotlenku, musisz znać wartościowość metalu. Ilość grup OH⁻ musi być równa wartościowości metalu, aby związek był elektrycznie obojętny.
Przykład: Wapń (Ca) ma wartościowość II. Grupa wodorotlenowa ma wartościowość I. Zatem potrzebujemy dwóch grup OH⁻, aby zrównoważyć ładunek wapnia. Stąd wzór wodorotlenku wapnia to Ca(OH)₂.
Właściwości wodorotlenków
Właściwości wodorotlenków zależą od metalu, z którym są połączone. Jednak niektóre cechy są wspólne:
- Stan skupienia: W temperaturze pokojowej są to zazwyczaj ciała stałe.
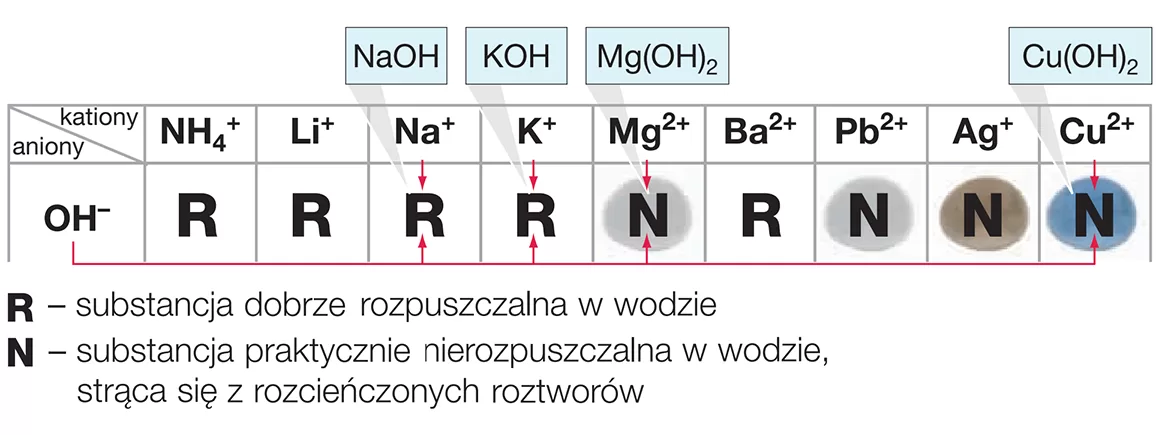
- Rozpuszczalność: Nie wszystkie wodorotlenki dobrze rozpuszczają się w wodzie. Te, które się rozpuszczają, nazywamy zasadami.
- Odczyn: Wodorotlenki mają odczyn zasadowy. Oznacza to, że w roztworze wodnym powodują, że papierek wskaźnikowy zmienia kolor na niebieski.
- Reakcje: Wodorotlenki reagują z kwasami, tworząc sól i wodę (reakcja zobojętniania).
Zasady - Rozpuszczalne wodorotlenki
Zasady to wodorotlenki metali alkalicznych (grupa 1 układu okresowego) i niektórych metali ziem alkalicznych (grupa 2 układu okresowego), które dobrze rozpuszczają się w wodzie. Przykłady zasad:
- NaOH (wodorotlenek sodu) - Soda kaustyczna, stosowana w przemyśle, np. do produkcji mydła.
- KOH (wodorotlenek potasu) - Potas kaustyczny, również stosowany w produkcji mydła, ale dającego mydło "miękkie".
- Ca(OH)₂ (wodorotlenek wapnia) - Wapno gaszone, stosowane w budownictwie i rolnictwie.
Uwaga! Zasady są żrące i mogą powodować poważne oparzenia. Należy zachować szczególną ostrożność podczas pracy z nimi.
Zastosowania wodorotlenków
Wodorotlenki mają szerokie zastosowanie w różnych dziedzinach:
- Przemysł chemiczny: Produkcja mydła, detergentów, papieru, włókien sztucznych.
- Budownictwo: Produkcja cementu, wapna.
- Rolnictwo: Wapnowanie gleby (regulacja pH gleby).
- Oczyszczanie ścieków: Neutralizacja kwasów.
- Lecznictwo: Niektóre wodorotlenki są składnikami leków (np. wodorotlenek glinu w lekach zobojętniających kwas żołądkowy).
- Przemysł spożywczy: Regulacja kwasowości w procesach produkcyjnych.
Wpływ na środowisko
Produkcja i stosowanie wodorotlenków, jak każdego związku chemicznego, może mieć wpływ na środowisko. Na przykład, niekontrolowane uwalnianie zasad do środowiska może prowadzić do skażenia wód i gleb. Dlatego ważne jest przestrzeganie zasad bezpieczeństwa i dbałość o środowisko.
Wodorotlenki - trudności i kontrargumenty
Częstym problemem dla uczniów jest rozróżnienie między wodorotlenkami i tlenkami. Pamiętaj, że wodorotlenki zawierają grupę OH⁻, a tlenki zawierają tylko atom tlenu (O). To podstawowa różnica.
Niektórzy mogą argumentować, że chemia jest niepotrzebna i nie ma zastosowania w życiu codziennym. To nieprawda! Chemia jest wszędzie! Zrozumienie podstaw chemii pozwala nam lepiej rozumieć świat i podejmować świadome decyzje dotyczące naszego zdrowia i środowiska.
Co dalej?
Mam nadzieję, że ten artykuł pomógł Ci zrozumieć podstawy dotyczące wodorotlenków. Pamiętaj, że kluczem do sukcesu w chemii jest systematyczna nauka i rozwiązywanie zadań. Nie bój się pytać nauczyciela o pomoc, jeśli czegoś nie rozumiesz.
Spróbuj wykonać kilka zadań z podręcznika lub zeszytu ćwiczeń. Zwróć uwagę na nazewnictwo wodorotlenków, pisanie wzorów chemicznych i właściwości. Im więcej ćwiczysz, tym lepiej to zrozumiesz.
Zastanów się: W jaki sposób znajomość chemii, a w szczególności wiedza o wodorotlenkach, może pomóc Ci w codziennym życiu lub w przyszłej karierze?