Bilansowanie Reakcji Chemicznych Klasa 7

Hej! Rozumiem, reakcje chemiczne i ich bilansowanie w 7 klasie potrafią sprawić trochę kłopotów. Te symbole, liczby, strzałki... To wszystko może wydawać się na początku bardzo skomplikowane. Ale spokojnie, nikt nie rodzi się z umiejętnością bilansowania równań chemicznych! To umiejętność, którą można opanować dzięki ćwiczeniom i odpowiedniemu podejściu. W tym artykule postaram się wytłumaczyć wszystko krok po kroku, tak żebyś zrozumiał(a) zasady i bez problemu radził sobie z zadaniami.
Co to w ogóle jest reakcja chemiczna?
Zacznijmy od podstaw. Reakcja chemiczna to po prostu proces, w którym jedne substancje (substraty) przekształcają się w inne substancje (produkty). Przykład? Spalanie drewna. Drewno (substrat) reaguje z tlenem (substrat) z powietrza, a w wyniku tej reakcji powstaje popiół, dwutlenek węgla i woda (produkty).
Reakcje chemiczne zapisujemy za pomocą równań. To taki chemiczny zapis, w którym wykorzystujemy symbole pierwiastków i wzory związków chemicznych. Na przykład:
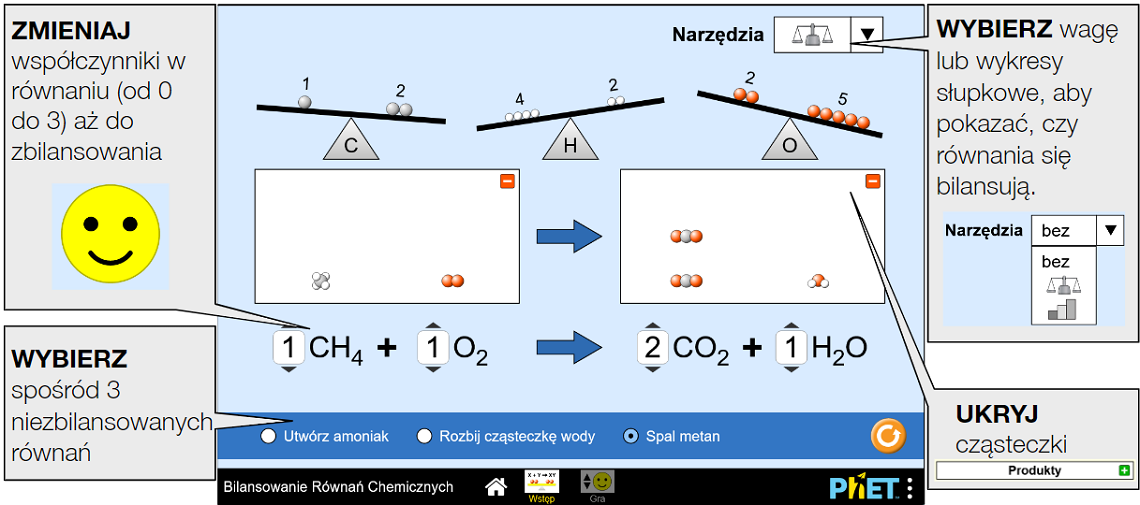
CH4 + 2O2 → CO2 + 2H2O
Ten zapis oznacza, że metan (CH4) reaguje z tlenem (O2), dając dwutlenek węgla (CO2) i wodę (H2O). Strzałka (→) oznacza kierunek reakcji.
Dlaczego musimy bilansować reakcje?
Teraz najważniejsze pytanie: dlaczego musimy bilansować te równania? Odpowiedź jest prosta: musi się zgadzać ilość atomów każdego pierwiastka po obu stronach równania. To wynika z prawa zachowania masy. Mówi ono, że w reakcji chemicznej masa substratów jest równa masie produktów. Innymi słowy, atomy nie znikają i nie pojawiają się magicznie – one tylko zmieniają swoje połączenia.
Wyobraź sobie, że budujesz domek z klocków. Masz 10 klocków czerwonych i 5 niebieskich. Po zbudowaniu domku nadal musisz mieć 10 klocków czerwonych i 5 niebieskich, tylko mogą być one ułożone w inny sposób. Tak samo jest z atomami w reakcji chemicznej.
Brak zbilansowania równania chemicznego oznaczałby, że atomy gdzieś zniknęły lub się pojawiły, co jest niezgodne z prawami fizyki.
Jak bilansować reakcje chemiczne? Krok po kroku
Okej, przejdźmy do konkretów. Jak bilansować reakcje chemiczne? Istnieje kilka metod, ale najpopularniejsza i najprostsza na początek to metoda prób i błędów. Spokojnie, brzmi groźnie, ale w rzeczywistości to nic trudnego!
Oto kroki, które należy wykonać:
Krok 1: Zapisz nie zbilansowane równanie reakcji.
Upewnij się, że poprawnie zapisałeś wzory chemiczne substratów i produktów.
Krok 2: Policz atomy każdego pierwiastka po obu stronach równania.
Zrób sobie tabelkę lub po prostu zapisz na kartce, ile atomów każdego pierwiastka znajduje się po stronie substratów, a ile po stronie produktów.
Krok 3: Dobierz współczynniki stechiometryczne.
Współczynniki stechiometryczne to liczby, które piszemy przed wzorami związków chemicznych. Mnożą one liczbę atomów danego pierwiastka w danym związku. Dobieramy je tak, aby liczba atomów każdego pierwiastka była taka sama po obu stronach równania. Pamiętaj, nigdy nie zmieniamy wzorów chemicznych związków!
Zaczynamy od pierwiastków, które występują tylko w jednym związku po stronie substratów i w jednym związku po stronie produktów. Często (ale nie zawsze!) dobrze jest zacząć od metali.
Krok 4: Sprawdź, czy równanie jest zbilansowane.
Po dobraniu współczynników ponownie policz atomy każdego pierwiastka po obu stronach równania. Jeśli liczby się zgadzają, gratulacje! Równanie jest zbilansowane. Jeśli nie, powtórz krok 3, aż osiągniesz sukces.
Przykład: Synteza wody
Przećwiczmy to na konkretnym przykładzie. Zbilansujmy równanie syntezy wody:
H2 + O2 → H2O
Krok 1: Mamy już zapisane nie zbilansowane równanie.
Krok 2: Policzmy atomy:
* Po stronie substratów: 2 atomy wodoru (H) i 2 atomy tlenu (O) * Po stronie produktów: 2 atomy wodoru (H) i 1 atom tlenu (O)Widzimy, że liczba atomów wodoru się zgadza, ale liczba atomów tlenu nie. Po stronie substratów mamy 2 atomy tlenu, a po stronie produktów tylko 1.
Krok 3: Dobierzmy współczynniki. Żeby po stronie produktów mieć 2 atomy tlenu, musimy pomnożyć wzór wody (H2O) przez 2:
H2 + O2 → 2H2O
Teraz mamy:
* Po stronie substratów: 2 atomy wodoru (H) i 2 atomy tlenu (O) * Po stronie produktów: 4 atomy wodoru (H) i 2 atomy tlenu (O)Ups! Teraz zgadza się liczba atomów tlenu, ale nie zgadza się liczba atomów wodoru. Po stronie produktów mamy 4 atomy wodoru, a po stronie substratów tylko 2. Musimy więc pomnożyć wzór wodoru (H2) po stronie substratów przez 2:
2H2 + O2 → 2H2O
Krok 4: Sprawdźmy, czy równanie jest zbilansowane:
* Po stronie substratów: 4 atomy wodoru (H) i 2 atomy tlenu (O) * Po stronie produktów: 4 atomy wodoru (H) i 2 atomy tlenu (O)Bingo! Liczba atomów każdego pierwiastka jest taka sama po obu stronach równania. Równanie jest zbilansowane.
Kilka dodatkowych wskazówek
* Ćwicz, ćwicz, ćwicz! Im więcej będziesz bilansować równań chemicznych, tym lepiej Ci to będzie wychodzić. * Zacznij od prostych równań. Na początku nie rzucaj się na trudne reakcje z wieloma pierwiastkami. Zacznij od prostych przykładów, a potem stopniowo zwiększaj poziom trudności. * Sprawdzaj swoje odpowiedzi. Po zbilansowaniu równania zawsze sprawdź, czy liczba atomów każdego pierwiastka jest taka sama po obu stronach. * Nie bój się prosić o pomoc. Jeśli masz problem z zbilansowaniem jakiegoś równania, poproś o pomoc nauczyciela, kolegę lub kogoś z rodziny, kto zna się na chemii. * Pamiętaj o ułamkach! Czasami, aby zbilansować równanie, trzeba użyć ułamków jako współczynników. Na przykład:C + 1/2 O2 → COJednak zazwyczaj chcemy mieć współczynniki będące liczbami całkowitymi. W takim przypadku mnożymy całe równanie przez 2:
2C + O2 → 2CO* Grupowanie atomów: W niektórych reakcjach występują grupy atomów, które pozostają niezmienione podczas reakcji (np. grupy siarczanowe SO42-). W takich przypadkach wygodnie jest traktować je jako jedną całość podczas bilansowania.
Dlaczego to się liczy?
Może się zastanawiasz, po co w ogóle uczyć się bilansowania reakcji chemicznych. Przecież to tylko symbole i liczby! Otóż, umiejętność bilansowania reakcji chemicznych jest kluczowa w wielu dziedzinach nauki i przemysłu.
- Chemia: Bez bilansowania nie można obliczyć ilości substancji potrzebnych do przeprowadzenia reakcji, ani przewidzieć ilości produktów, które powstaną.
- Farmacja: W produkcji leków bardzo ważne jest, aby dokładnie odmierzyć ilości składników i kontrolować przebieg reakcji chemicznych.
- Ochrona środowiska: Zrozumienie reakcji chemicznych zachodzących w atmosferze i glebie pozwala nam walczyć z zanieczyszczeniami i dbać o naszą planetę.
Podsumowując, bilansowanie reakcji chemicznych to ważna umiejętność, która otwiera drzwi do zrozumienia świata wokół nas. Nie zrażaj się początkowymi trudnościami! Z odrobiną wysiłku i ćwiczeń na pewno opanujesz tę sztukę.
Powodzenia!