Atomy I Cząsteczki Chemia Klasa 7

Witajcie w fascynującym świecie Atomy i cząsteczek, podstawowych elementów chemii, które poznajemy już w 7 klasie! Ten artykuł ma za zadanie wprowadzić Was w temat atomy, cząsteczki i ich fundamentalne znaczenie w zrozumieniu otaczającego nas świata. Zrozumienie tych pojęć jest kluczowe, ponieważ wszystko, co widzimy, dotykamy i czego doświadczamy, składa się z atomów i cząsteczek.
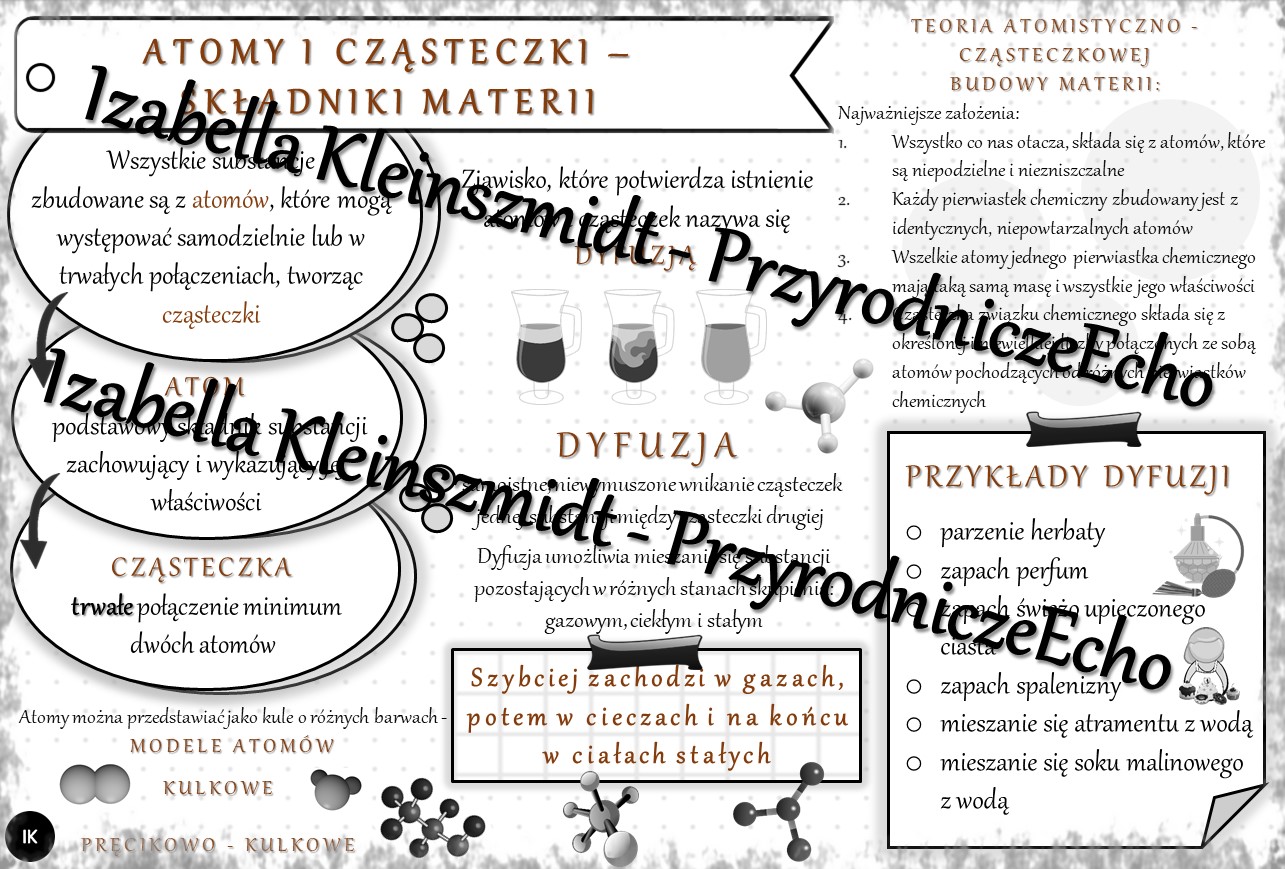
Atom - Fundament Materii
Atom jest najmniejszą jednostką pierwiastka chemicznego, która zachowuje jego właściwości chemiczne. Wyobraźcie sobie, że bierzecie kawałek złota i dzielicie go na coraz mniejsze części. W pewnym momencie dotrzecie do atomu złota. Jeśli spróbujecie go podzielić dalej, stracicie właściwości złota.
Struktura atomu
Atom składa się z jądra i krążących wokół niego elektronów. Jądro zawiera protony (ładunek dodatni) i neutrony (ładunek obojętny). Elektrony (ładunek ujemny) poruszają się po określonych poziomach energetycznych zwanych orbitalami. Ilość protonów w jądrze decyduje o tym, jakim pierwiastkiem jest dany atom. Na przykład, atom węgla ma 6 protonów, atom tlenu ma 8 protonów, a atom wodoru ma tylko 1 proton. Liczba neutronów może się różnić, tworząc izotopy danego pierwiastka.
Przykład: Atom węgla-12 (12C) ma 6 protonów i 6 neutronów, natomiast atom węgla-14 (14C) ma 6 protonów i 8 neutronów. Oba są atomami węgla, ale różnią się masą.
Zapamiętaj: Protony determinują, jakim pierwiastkiem jest atom, a elektrony decydują o jego właściwościach chemicznych, czyli o tym, jak atom będzie łączył się z innymi atomami.
Cząsteczka - Zbiór Atomów
Cząsteczka powstaje, gdy dwa lub więcej atomów połączy się ze sobą za pomocą wiązań chemicznych. Te wiązania chemiczne powstają dzięki interakcji elektronów między atomami. Cząsteczki mogą być bardzo proste, jak na przykład cząsteczka wodoru (H2), która składa się z dwóch atomów wodoru, lub bardzo złożone, jak na przykład cząsteczki DNA, które zawierają miliony atomów węgla, wodoru, tlenu, azotu i fosforu.
Rodzaje cząsteczek
Możemy wyróżnić dwa główne rodzaje cząsteczek:
* Związki chemiczne: Cząsteczki składające się z różnych rodzajów atomów. Na przykład, woda (H2O) to związek chemiczny, ponieważ składa się z atomów wodoru i tlenu. Dwutlenek węgla (CO2) to także związek chemiczny, składający się z atomów węgla i tlenu. * Pierwiastki: Cząsteczki składające się z tego samego rodzaju atomów. Na przykład, tlen (O2) to pierwiastek, ponieważ składa się tylko z atomów tlenu. Azot (N2) to także pierwiastek, składający się tylko z atomów azotu.Przykład: Woda (H2O) jest niezbędna do życia. Dzięki swoim unikalnym właściwościom, umożliwia transport substancji odżywczych, reguluje temperaturę i bierze udział w wielu procesach biologicznych.
Zapamiętaj: Wiązania chemiczne "trzymają" atomy razem w cząsteczce. Rodzaj wiązania chemicznego wpływa na właściwości cząsteczki.
Właściwości Materii a Atomy i Cząsteczki
Wszystkie właściwości materii, które obserwujemy na co dzień, są bezpośrednio związane z rodzajem atomów i rodzajem cząsteczek, z których dana substancja się składa, oraz z ich układem. Na przykład:
* Stan skupienia: Czy substancja jest ciałem stałym, cieczą czy gazem, zależy od sił, jakie działają między cząsteczkami. W ciałach stałych cząsteczki są ściśle upakowane i mocno ze sobą związane. W cieczach cząsteczki są bliżej siebie niż w gazach, ale mogą się przemieszczać. W gazach cząsteczki są daleko od siebie i poruszają się swobodnie. * Temperatura wrzenia i topnienia: Temperatura, w której dana substancja zmienia stan skupienia, zależy od siły wiązań między cząsteczkami. Im silniejsze wiązania, tym wyższa temperatura wrzenia i topnienia. * Przewodnictwo elektryczne: Substancje, które dobrze przewodzą prąd elektryczny (np. metale), mają atomy, które łatwo oddają elektrony. Substancje, które nie przewodzą prądu elektrycznego (np. plastik), mają atomy, które trzymają elektrony bardzo mocno. * Rozpuszczalność: To, czy dana substancja rozpuszcza się w innej substancji, zależy od tego, jak podobne są do siebie cząsteczki obu substancji. Na przykład, woda (H2O) dobrze rozpuszcza sól (NaCl), ponieważ oba związki są polarne (mają nierównomierny rozkład ładunku).Przykład: Diament i grafit, obie substancje zbudowane są wyłącznie z atomów węgla. Jednak diament jest bardzo twardy i bezbarwny, a grafit jest miękki i czarny. Ta różnica wynika z różnego układu atomów węgla w obu substancjach. W diamencie atomy węgla są połączone w bardzo mocną sieć krystaliczną, a w graficie atomy węgla są ułożone w warstwy, które łatwo się ślizgają po sobie.
Atomy i cząsteczki w codziennym życiu
Wszechobecność atomów i cząsteczek czyni je niezwykle ważnymi w naszym codziennym życiu. Oto kilka przykładów:
* Leki: Wszystkie leki, które zażywamy, to związki chemiczne składające się z określonych atomów i cząsteczek. Działają one poprzez interakcję z określonymi cząsteczkami w naszym organizmie. * Materiały budowlane: Beton, stal, drewno – wszystkie te materiały zbudowane są z różnych atomów i cząsteczek, które nadają im określone właściwości (wytrzymałość, twardość, elastyczność). * Żywność: Wszystko, co jemy, składa się z atomów i cząsteczek. Białka, węglowodany, tłuszcze, witaminy – wszystkie te składniki odżywcze są związkami chemicznymi o złożonej strukturze. * Paliwa: Benzyna, olej napędowy, gaz ziemny – wszystkie te paliwa są związkami chemicznymi, które uwalniają energię podczas spalania.Dlaczego warto zrozumieć chemię atomów i cząsteczek?
Zrozumienie chemii atomów i cząsteczek otwiera drzwi do zrozumienia całego otaczającego nas świata. Pozwala nam zrozumieć, jak działają różne procesy chemiczne, dlaczego pewne substancje mają takie, a nie inne właściwości, i jak możemy wykorzystywać chemię do rozwiązywania problemów i tworzenia nowych technologii.
Przykładowe zastosowania wiedzy o atomach i cząsteczkach:
* Ochrona środowiska: Zrozumienie, jak zanieczyszczenia wpływają na środowisko, pozwala nam opracowywać skuteczne metody ich usuwania i zapobiegania. * Medycyna: Opracowywanie nowych leków i terapii, które skutecznie leczą choroby. * Energetyka: Poszukiwanie nowych źródeł energii, które są czyste i odnawialne. * Materiały: Tworzenie nowych materiałów o unikalnych właściwościach, które mogą być wykorzystywane w różnych dziedzinach (np. w elektronice, lotnictwie, medycynie).Podsumowanie i Dalsze Kroki
Atomy i cząsteczki to podstawa całej materii. Zrozumienie ich budowy i właściwości jest kluczowe do zrozumienia chemii i otaczającego nas świata. Pamiętaj, że:
* Atom to najmniejsza jednostka pierwiastka. * Cząsteczka powstaje, gdy atomy łączą się ze sobą. * Właściwości materii zależą od rodzaju atomów i cząsteczek oraz ich układu.Zachęcam Was do dalszego zgłębiania wiedzy o atomach i cząsteczkach. Czytajcie książki, oglądajcie filmy edukacyjne, przeprowadzajcie eksperymenty (oczywiście pod nadzorem osoby dorosłej!). Chemia jest fascynującą dziedziną nauki, która otwiera drzwi do zrozumienia świata i tworzenia przyszłości!
Zadanie dla Ciebie: Poszukaj w swoim otoczeniu przedmiotów i spróbuj zastanowić się, z jakich atomów i cząsteczek mogą być zbudowane. Jakie właściwości mają te przedmioty i jak są one związane z budową ich cząsteczek? Powodzenia!