Alkohole I Kwasy Karboksylowe Sprawdzian Kl 8
Ten artykuł został napisany z myślą o uczniach klasy ósmej przygotowujących się do sprawdzianu z alkoholi i kwasów karboksylowych. Naszym celem jest uporządkowanie wiedzy, wyjaśnienie kluczowych zagadnień i dostarczenie praktycznych wskazówek, które pomogą Ci zdać egzamin śpiewająco!
Zastanawiałeś się kiedyś, co sprawia, że ocet ma tak kwaśny smak? Albo dlaczego alkohol ma działanie odurzające? Odpowiedź leży w tajemniczym świecie chemii organicznej, a konkretnie w związkach zwanych alkoholami i kwasami karboksylowymi. Zapnij pasy, ruszamy w fascynującą podróż!
Alkohole: Co to takiego i gdzie je znajdziemy?
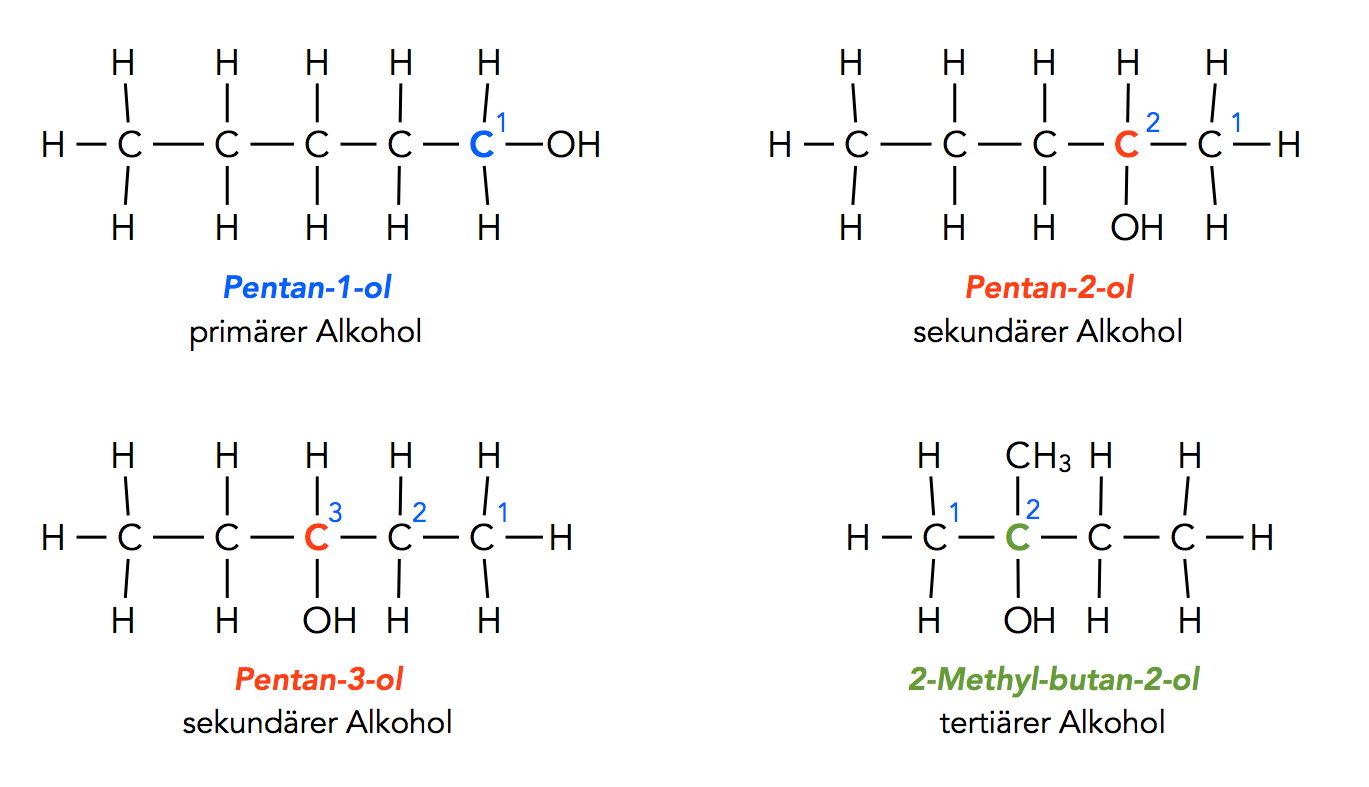
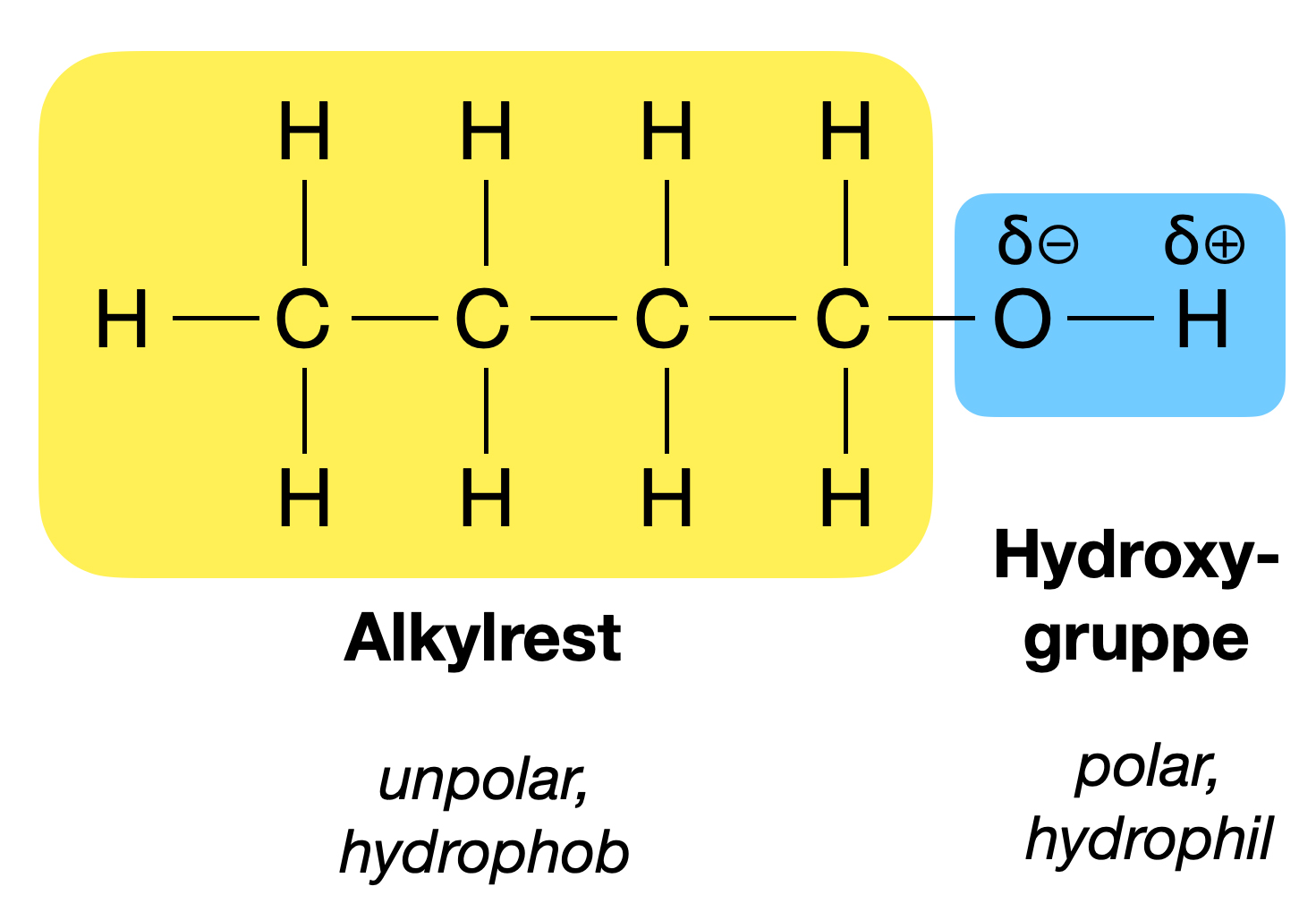
Alkohole to organiczne związki chemiczne, które w swojej strukturze zawierają grupę hydroksylową (-OH). Ta mała, ale ważna grupa, decyduje o ich właściwościach.
Podział i nazewnictwo alkoholi
Alkohole dzielimy w zależności od liczby grup hydroksylowych w cząsteczce:
- Alkohole monohydroksylowe: Zawierają jedną grupę -OH (np. metanol, etanol).
- Alkohole polihydroksylowe: Zawierają więcej niż jedną grupę -OH (np. glikol, glicerol).
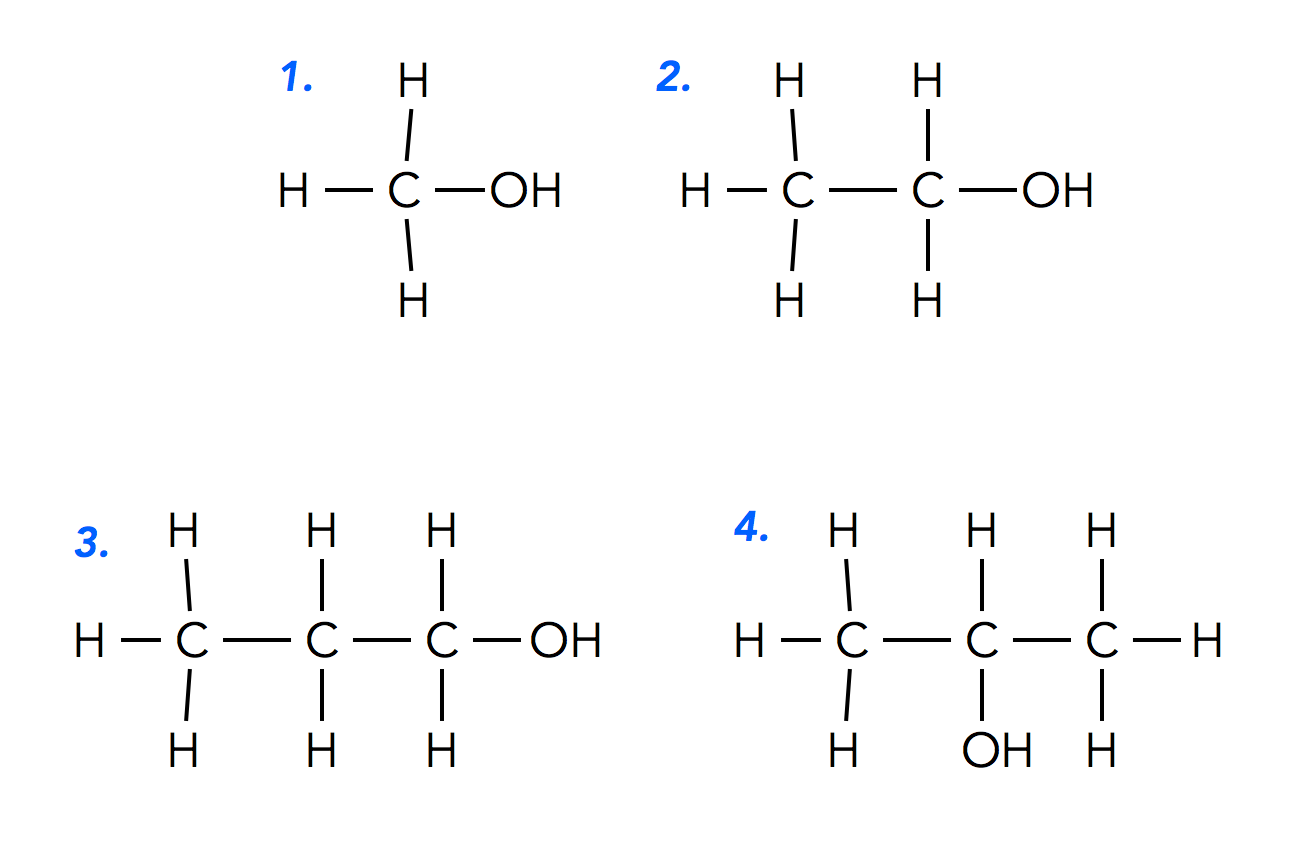
Nazewnictwo alkoholi jest dość proste: do nazwy alkanu (węglowodoru) o tej samej liczbie atomów węgla dodajemy końcówkę "-ol". Na przykład:
- Metan → Metanol (CH3OH)
- Etan → Etanol (C2H5OH)
- Propan → Propanol (C3H7OH)
Właściwości alkoholi
Właściwości fizyczne i chemiczne alkoholi zależą od długości łańcucha węglowego i obecności grupy hydroksylowej:
- Rozpuszczalność: Alkohole o krótkich łańcuchach węglowych dobrze rozpuszczają się w wodzie. Wraz ze wzrostem długości łańcucha węglowego, rozpuszczalność maleje.
- Temperatura wrzenia: Alkohole mają wyższe temperatury wrzenia niż odpowiadające im alkany, ze względu na tworzenie wiązań wodorowych między cząsteczkami.
- Reakcje: Alkohole uczestniczą w różnych reakcjach chemicznych, np. w reakcjach spalania, utleniania i estryfikacji.
Zastosowanie alkoholi
Alkohole mają szerokie zastosowanie w różnych dziedzinach:
- Etanol: Stosowany jako rozpuszczalnik, składnik napojów alkoholowych, paliwo, środek dezynfekujący.
- Metanol: Stosowany jako rozpuszczalnik, surowiec do produkcji innych związków chemicznych. Uwaga: Metanol jest silnie toksyczny!
- Glicerol: Stosowany w kosmetyce (nawilżanie skóry), przemyśle spożywczym (jako dodatek do żywności).
Kwasy karboksylowe: Źródło kwaśnego smaku!
Kwasy karboksylowe to organiczne związki chemiczne, które zawierają grupę karboksylową (-COOH). To właśnie obecność tej grupy nadaje im charakterystyczne kwaśne właściwości.
Podział i nazewnictwo kwasów karboksylowych
Kwasy karboksylowe dzielimy na:
- Kwasy alifatyczne: Zawierają łańcuch węglowy (np. kwas mrówkowy, kwas octowy).
- Kwasy aromatyczne: Zawierają pierścień aromatyczny (np. kwas benzoesowy).
Nazewnictwo kwasów karboksylowych jest podobne do nazewnictwa alkoholi, ale zaczyna się od słowa "kwas" i dodaje końcówkę "-owy". Na przykład:
- Metan → Kwas metanowy (H-COOH) - Kwas mrówkowy
- Etan → Kwas etanowy (CH3COOH) - Kwas octowy
- Propan → Kwas propanowy (C2H5COOH)
Właściwości kwasów karboksylowych
Właściwości kwasów karboksylowych zależą od długości łańcucha węglowego i obecności grupy karboksylowej:
- Kwasowość: Kwasy karboksylowe są kwasami słabymi, co oznacza, że w roztworach wodnych ulegają częściowej dysocjacji na jony.
- Rozpuszczalność: Kwasy o krótkich łańcuchach węglowych dobrze rozpuszczają się w wodzie. Wraz ze wzrostem długości łańcucha węglowego, rozpuszczalność maleje.
- Reakcje: Kwasy karboksylowe reagują z alkoholami, tworząc estry (reakcja estryfikacji).
Zastosowanie kwasów karboksylowych
Kwasy karboksylowe mają szerokie zastosowanie w różnych dziedzinach:
- Kwas octowy: Stosowany jako ocet spożywczy, surowiec do produkcji tworzyw sztucznych, leków.
- Kwas cytrynowy: Stosowany jako dodatek do żywności (regulator kwasowości, konserwant).
- Kwas mrówkowy: Stosowany w garbarstwie, przemyśle tekstylnym, jako środek konserwujący.
Reakcja estryfikacji: Połączenie alkoholu i kwasu
Reakcja estryfikacji to reakcja chemiczna, w której alkohol reaguje z kwasem karboksylowym, w wyniku czego powstaje ester i woda. Jest to reakcja odwracalna i zachodzi w obecności katalizatora (np. kwasu siarkowego).
Kwas karboksylowy + Alkohol → Ester + Woda
Estry mają często przyjemne zapachy i są wykorzystywane w przemyśle perfumeryjnym i spożywczym (jako aromaty). Na przykład, octan etylu ma zapach gruszek.
Przygotowanie do sprawdzianu: Praktyczne wskazówki
- Powtórz definicje: Upewnij się, że rozumiesz, co to są alkohole i kwasy karboksylowe.
- Naucz się nazewnictwa: Ćwicz nazywanie różnych alkoholi i kwasów karboksylowych.
- Zrozum właściwości: Przemyśl, dlaczego alkohole i kwasy karboksylowe mają takie, a nie inne właściwości.
- Przeanalizuj reakcje: Zrozum, jak zachodzi reakcja estryfikacji i jakie są jej produkty.
- Rozwiąż zadania: Ćwicz rozwiązywanie zadań obliczeniowych i problemowych związanych z alkoholami i kwasami karboksylowymi.
- Użyj fiszek: Stwórz fiszki z najważniejszymi informacjami i regularnie je powtarzaj.
- Poproś o pomoc: Jeśli masz jakieś pytania, nie bój się zapytać nauczyciela lub kolegów.
Pamiętaj, że kluczem do sukcesu jest systematyczna nauka i zrozumienie materiału. Nie ucz się na pamięć, staraj się zrozumieć zasady rządzące chemią organiczną. Powodzenia na sprawdzianie! Jesteśmy pewni, że dasz z siebie wszystko!


/model-of-ethanol--c2h5oh--molecule--close-up-90116746-5a56272b482c520037e24cec.jpg)
